
 ��ѧ��Ӧ�����뻯ѧƽ��
��ѧ��Ӧ�����뻯ѧƽ��| �¶� | 250�� | 300�� | 350�� |
| K | 2.041 | 0.270 | 0.012 |
| ��ʵ���� | ��T���棩 | $\frac{n��CO��}{n��{H}_{2}��}$ | ��P��MPa�� |
| ��i | ��150 | $\frac{1}{3}$ | ��0.1 |
| ��ii | 150 | $\frac{1}{3}$ | 5 |
| ��iii | ��350 | $\frac{1}{3}$ | ��5 |
���� ��һ�����ݻ�ѧƽ������ʽ��ʽ���㣬C�����ʵ���=1.2mol/L��2L=2��4mol��
2A��g��+B��g��?xC��g��+2D��s����
��ʼ����mol�� 2 2 0 0
�仯����mol�� 1.6 0.8 0.8x 1.6
ƽ������mol�� 0.4 1.2 2.4 1.6
0.8x=2.4��x=3������v��A��=$\frac{��c}{��t}$���㣻
��1��������ƽ�ⳣ�����¶ȱ仯�������¶�Խ��ƽ�ⳣ��ԽС��˵��ƽ��������У�
������Ũ���̺�ƽ�ⳣ���ȽϷ����жϷ�Ӧ���еķ���
��������1�����ɱ������ݿ�֪���¶�Խ�ߣ�ƽ�ⳣ��ԽС��˵�������¶�ƽ�����淴Ӧ�ƶ������ݷ�Ӧ�Է����е��ж����ݷ�����
�ڼ����ʱ��Ũ����Qc����ƽ�ⳣ���Ƚϣ��жϷ�Ӧ���еķ���
�۸�ͬѧͨ�������Ʊ�������̽����������Ի�ѧƽ���Ӱ�죬̽����ǰ��ֻ���Ǹı�һ���������������������䣬�ݴ˽��
�������¶Ȳ��䣬��ѧƽ�ⳣ�����䣬�������̼Ũ�Ȳ��䣬����PV=nRT�ж�ƽ������ѹǿ��
��� �⣺��һ�����ݻ�ѧƽ������ʽ��ʽ���㣬C�����ʵ���=1.2mol/L��2L=2��4mol��
2A��g��+B��g��?xC��g��+2D��s����
��ʼ����mol�� 2 2 0 0
�仯����mol�� 1.6 0.8 0.8x 1.6
ƽ������mol�� 0.4 1.2 2.4 1.6
0.8x=2.4��x=3��
��1������v��A��=$\frac{��c}{��t}$��֪��A���ĵ�ƽ����Ӧ����Ϊ$\frac{\frac{1.6mol}{2L}}{2min}$=0.4mol/��L•min����
�ʴ�Ϊ��0.4mol/��L•min����
��2��������ķ�����֪��x=3��
�ʴ�Ϊ��3��
��������1�����ɱ������ݿ�֪���¶�Խ�ߣ�ƽ�ⳣ��ԽС��˵�������¶�ƽ�����淴Ӧ�ƶ���������ӦΪ���ȷ�Ӧ������H��0��CO��g��+2H2��g��?CH3OH��g������Ӧ��H��0����S��0�����ݷ�Ӧ�Է����У���H-T��S��0�����������·�Ӧ�Է����У�
�ʴ�Ϊ�������ϵͣ�
�ڡ���2mol CO��3mol H2��2mol CH3OH�����ݻ�Ϊ1L���ܱ������У���ʱ��Ũ����Qc=$\frac{2}{2��3{\;}^{2}}$=$\frac{1}{9}$��С��0.27���ʷ�Ӧ������Ӧ���У�
�ʴ�Ϊ��A��
��ͨ�������Ʊ�������̽����������Ի�ѧƽ���Ӱ�죬̽����ǰ��ֻ���Ǹı�һ���������������������䣬�ɴ˿ɵã�ii���¶�AΪ150�棬n ��CO��/n��H2��BΪ$\frac{1}{3}$��DΪ5��iii��n ��CO��/n��H2��CΪ$\frac{1}{3}$��
�ʴ�Ϊ��150��$\frac{1}{3}$��5��$\frac{1}{3}$��
�������¶Ȳ��䣬��ѧƽ�ⳣ�����䣬�������̼Ũ�Ȳ��䣬����PV=nRT֪��P=$\frac{n}{V}$RT=CRT���¶Ȳ��䣬R�dz�����C���䣬��P���䣬����t0ʱ�̺���ϵ��ѹǿ��p�����꣩
��ʱ�䣨t�����꣩�Ĺ�ϵͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���˻�ѧƽ�⡢ƽ�ⳣ��Ӱ�����ط����жϣ�ƽ���־������Ӧ�ã�ע���Чƽ��״̬�ķ���Ӧ�ã����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�갲��ʡ�߶��ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�¶��£�H2��g��+CO2��g�� H2O��g��+CO��g����ƽ�ⳣ��K=
H2O��g��+CO��g����ƽ�ⳣ��K=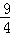 �����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2��g����CO2��g��������ʼŨ�������ʾ�������жϲ���ȷ���ǣ� ��
�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2��g����CO2��g��������ʼŨ�������ʾ�������жϲ���ȷ���ǣ� ��
��ʼŨ�� | �� | �� | �� |
c��H2��/mol/L | 0.010 | 0.020 | 0.020 |
c��CO2��/mol/L | 0.010 | 0.010 | 0.020 |
A�� ƽ��ʱ������CO2��ת���ʴ���60%
B�� ƽ��ʱ�����кͱ���H2��ת���ʾ���60%
C�� ƽ��ʱ������c��CO2���Ǽ��е�2������0.012mol/L
D�� ��Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�������Ͽ��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������Mg5Al3(OH)x(H2O)4������������ȼ���ϣ�����ʱ�ᷢ�����·ֽⷴӦ������M��ij�����ʣ�aΪ��ѧ����������2Mg5Al3(OH)x(H2O)4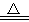 27H2O��+10M+aAl2O3����˵����ȷ����
27H2O��+10M+aAl2O3����˵����ȷ����
A��a=2
B��x=18
C��M�Ļ�ѧʽΪMgO
D���÷�Ӧ��Mg5Al3(OH)x(H2O)4�������������ǻ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�����ϵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
��ҵ����CuFeS2Ϊԭ��ұ��ͭ
 ����Ҫ��ӦΪ��2CuFeS2+4O2=Cu2S+3SO2+2FeO (¯������
����Ҫ��ӦΪ��2CuFeS2+4O2=Cu2S+3SO2+2FeO (¯������
��2Cu2S+3O2= 2Cu2O+2SO2;��2Cu2O+Cu2S=6Cu+SO2������˵��������ǣ� ��
2Cu2O+2SO2;��2Cu2O+Cu2S=6Cu+SO2������˵��������ǣ� ��
A���� 1 mol CuFeS2 ���� 1mol Cu�������� 2.75 molO2
B����ұ�������в����������к�����SO2,�ɻ��������Ʊ�����
C���ڷ�Ӧ���У�Cu2S���������������ǻ�ԭ��
D���ڷ�Ӧ���У�SO2��������������ǻ�ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�����ϵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
��п������ͭ��ĩ��һ���������Ͷ�뵽һ�����������У��ȣ���ַ�Ӧ����ˣ���ȥ��������Һ�� ��������������������ǣ� ��
A��ֻ�� Cu2 +��Fe2+��Zn2+ B��ֻ�� Zn2+
+��Fe2+��Zn2+ B��ֻ�� Zn2+
C��ֻ�� Fe2+��Zn2+ D��ֻ�� Cu2+��Fe3+��Zn2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
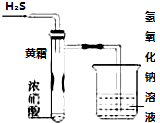 ijͬѧ������ʵ��װ��̽����������ʣ�����ͼʾ�ж����н��۲���ȷ����
ijͬѧ������ʵ��װ��̽����������ʣ�����ͼʾ�ж����н��۲���ȷ����| A�� | �Թ��ڱ��ϡ���˪���ijɷ����� | |
| B�� | ��ʵ��̽��˵��Ũ������������ԣ����лӷ��� | |
| C�� | �ձ��ڵ�NaOH��Һ�������dz�ȥβ������ֹβ����Ⱦ���� | |
| D�� | H2S��SO2���棬�������Է�Ӧ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܣ��ۣ��ڣ��� | B�� | �ۣ��ܣ��ڣ��� | C�� | �ڣ��ۣ��ܣ��� | D�� | �ۣ��ڣ��ܣ��� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com