
【题目】下列物质在给定条件下的同分异构体数目正确的是( )
A. C4H10属于烷烃的同分异构体有3种
B. 分子组成是C5H10O2属于羧酸的同分异构体有5种
C. 分子组成是C4H8O属于醛的同分异构体有3种
D. 结构简式为![]() 的一溴代物有5种
的一溴代物有5种
科目:高中化学 来源: 题型:
【题目】乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。回答下列问题:
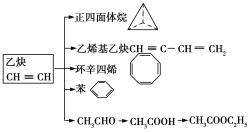
(1)正四面体烷的二氯取代产物有_____种。
A.1种 B.2种 C.3种 D.4种
(2)关于乙烯基乙炔分子的说法错误的是____(填字母符号)。
A.能使酸性KMnO4溶液褪色
B.1 mol乙烯基乙炔最多能与3 mol Br2发生加成反应
C.乙烯基乙炔分子内含有两种官能团
D.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量不相同
E.乙烯基乙炔分子中的所有原子一定都共平面
(3)环辛四烯的分子式为____,写出与环辛四烯互为同分异构体且属于芳香烃的分子的结构简式:_______
(4)下列属于苯的同系物的是____(填字母符号)。
A.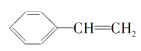 B.
B.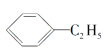
C.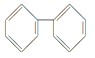 D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(N2H4)又称肼,是一种良好的火箭燃料,与适量氧化剂混合可组成液体推进剂,无水N2H4液体有微弱氨气的气味。
(1)N2(g)+2O2(g)=2NO2(g) ΔH1=+67.7 kJ/mol,N2H4(g)+O2(g)=N2(g)+2H2O(l) ΔH2=-622 kJ/mol,试计算1 mol气态肼与二氧化氮完全反应时放出的热量为_______。
(2)在加热条件下,液态肼可还原新制的Cu(OH)2制备纳米级Cu2O,并产生无污染气体,试写出该反应的化学反应方程式_______________________________。
(3)以气态肼为原料的碱性燃料电池的总反应为N2H4+O2=N2+2H2O,放电时负极的反应方程式为______________________________
(4)肼的性质与氨气相似,易溶于水,可发生两步电离过程,第一步电离过程 N2H4+H2O![]() N2H5++OH-,试写出第二步电离过程____________________________。常温下,某浓度N2H6Cl2溶液的pH为4,则该溶液中水电离出的c(H+)=_______________。
N2H5++OH-,试写出第二步电离过程____________________________。常温下,某浓度N2H6Cl2溶液的pH为4,则该溶液中水电离出的c(H+)=_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸是常见的无机强酸,是重要的化工原料。实验室模拟硝酸的制备可用以下装置,其中a为一个可持续鼓入空气的橡皮球,b、c为止水夹。

(1)实验开始前,应检验装置的气密性,请写出检验A~E装置(不必考虑a)的气密性方法________________。
(2)装置A中发生反应的化学方程式为___________。装置C中浓硫酸的作用是__________。
(3)实验进行一段时间,待制备一定量硝酸后,停止加热A和B中装置,但仍要通过a鼓入一定量的空气,该操作的目的是____________________。
(4)若F装置中所选用试剂为酸性KMnO4溶液,请写出F装置处理NO尾气的离子方程式:_____________________。
(5)欲使A中产生的氨气尽可能转化为硝酸,理论上氨气与鼓入空气的最佳比例为_______。
(6)实验完毕后,取E中的溶液,加入几滴酚酞溶液,用0.10 mol/L的NaOH标准液滴定,发现加入过量标准液后仍无现象,试解释没有观察到滴定终点的原因_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一瓶签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合制剂,某同学为了确认其成分,取部分制剂作为试液,设计并完成了如下实验:

已知:控制溶液pH=4时,Fe(OH)3沉淀完全,Ca2+、Mg2+不沉淀。
该同学得出的结论正确的是
A. 根据现象1可推出该试液中含有Na+
B. 根据现象2可推出该试液中并不含有葡萄糖酸根
C. 根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+
D. 根据现象5可推出该试液中一定含有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.如图所示,已知有机物A 的一种同系物的产量,是衡量一个国家石油化工水平的标志,且0.1mol A在足量的氧气中完全燃烧,生成0.3 mol CO2和0.3 mol水。B和D都是有机物,E是具有浓郁香味、不易溶于水的油状液体。
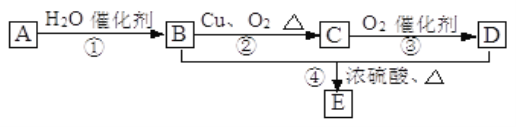
已知:-CHOH最终不能被氧化为—COOH
(1)写出A的结构简式_______。
(2)写出B的结构简式为_______,D中官能团的名称为_______。
(3)写出下列反应的类型:①_______,④_______。
(4)写出下列物质转化的化学方程式: B→C _________ ;B+D→E ______________。
Ⅱ.在实验室可以用如图所示的装置进行B与D的反应,请回答下列问题:

(1)装置中通蒸气的导管要在试管中液面的上方,该溶液的作用是_______。
(2)若要把制得的E分离出来,应采用的实验操作是_______。
Ⅲ. 苹果醋是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等药效。苹果酸是苹果醋的主要成分,其结构简式如图所示,请回答下列问题:
![]()
(1)在一定条件下,苹果酸可能与下列哪些物质发生反应?_______
A.氢氧化钠溶液 B.乙酸 C.碳酸氢钠溶液 D.乙醇
(2)0.1 mol苹果酸与足量金属钠反应,能生成标准状况下的氢气_______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。
请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
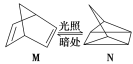 ΔH=+88.6 kJ·mol-1
ΔH=+88.6 kJ·mol-1
则M、N相比,较稳定的是 。
(2)已知CH3OH(l)的燃烧热为238.6 kJ·mol-1,CH3OH(l)+![]() O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a 238.6(填“>”、“<”或“=”)。
O2(g)=CO2(g)+2H2(g) ΔH=-a kJ·mol-1,则a 238.6(填“>”、“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式: 。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)=2Al2O3(s)+3TiC(s) ΔH=-1 176 kJ·mol-1,则反应过程中,每转移1 mol电子放出的热量为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常见金属A、B、C和常见气体甲、乙、丙及物质D、E、F、G、H,它们之间的转化关系如图所示,请根据以上信息回答下列问题:
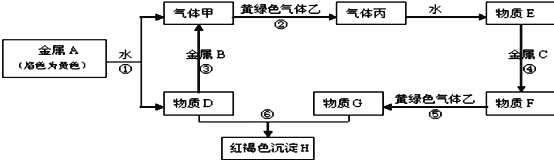
(1)写出下列物质的化学式:B _______ F______
(2)写出下列反应离子方程式:
反应⑤________________
反应⑥_______________
(3)实验室制取气体乙时,先将气体生成物通过 _______以除去_______
(4)在反应MnO2 + 4HCl(浓) △ MnCl2 + Cl2↑+ 2H2O中,浓盐酸体现了_____ 性和__________性,参加反应的氧化剂与还原剂的物质的量之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用浓盐酸和二氧化锰反应制取氯气,并经净化得干燥、纯将的氯气。
(1)某学生开列了下列实验用品:
实验仪器:铁架台、酒精灯、铁圈、铁夹、圆底烧瓶、双孔橡胶塞、分液漏斗、玻璃导管、橡皮管、洗气瓶(2个)、集气瓶、火柴。还缺少的仪器是________和_________。
试剂:二氧化锰、浓盐酸、氢氧化钠溶液。还缺少的试剂是__________。
(2)写出本实验中制取氯气反应的化学方程式______________________________。
(3)所列试剂中氢氧化钠的作用是______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com