
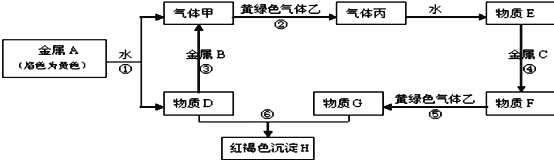
【题目】现有常见金属A、B、C和常见气体甲、乙、丙及物质D、E、F、G、H,它们之间的转化关系如图所示,请根据以上信息回答下列问题:
(1)写出下列物质的化学式:B _______ F______
(2)写出下列反应离子方程式:
反应⑤________________
反应⑥_______________
(3)实验室制取气体乙时,先将气体生成物通过 _______以除去_______
(4)在反应MnO2 + 4HCl(浓) △ MnCl2 + Cl2↑+ 2H2O中,浓盐酸体现了_____ 性和__________性,参加反应的氧化剂与还原剂的物质的量之比为_____。
【答案】Al FeCl2 2Fe2++Cl2 === 2Fe3++ 2Cl- Fe3++ 3OH- == Fe(OH)3↓ 饱和食盐水 HCl气体 还原性 酸性 1:2
【解析】
金属A焰色反应为黄色,故A为金属Na,由反应①可以知道,D为NaOH,气体甲为H2;氢氧化钠与金属B反应生成氢气,故金属B为Al。黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质E为盐酸。氢氧化钠与物质G反应生成红褐色沉淀是Fe(OH)3,故物质G中含有Fe3+,由转化关系HCl![]() 物质F
物质F![]() 物质G,可以知道金属C为Fe,物质F为FeCl2,物质G为FeCl3,结合物质的性质解答该题。
物质G,可以知道金属C为Fe,物质F为FeCl2,物质G为FeCl3,结合物质的性质解答该题。
(1)由以上分析可以知道,B为Al,F为FeCl2,
因此,本题正确答案是:Al ;FeCl2;
(2)反应⑤为氯化亚铁与氯气反应生成氯化铁,反应离子方程式为:2Fe2++Cl2 === 2Fe3++ 2Cl-;
反应(6)是氯化铁与氢氧化钠反应生成氢氧化铁沉淀与氯化钠,反应离子方程式为:Fe3++ 3OH- == Fe(OH)3↓;
因此,本题正确答案是:2Fe2++Cl2 === 2Fe3++ 2Cl- ;Fe3++ 3OH- == Fe(OH)3↓;
(3)实验室用二氧化锰和浓盐酸加热制Cl2时,氯气中混有HCl和水蒸气,要先将气体生成物通过饱和食盐水以除去HCl气体,
因此,本题正确答案是:饱和食盐水;HCl气体;
(4)在反应MnO2 + 4HCl(浓)![]() MnCl2 + Cl2↑+ 2H2O中,Mn元素的化合价降低,MnO2为氧化剂,部分Cl元素的化合价升高,则HCl为还原剂,浓盐酸体现了还原性和酸性,由电子守恒可知,氧化剂与还原剂的物质的量比为1:2,
MnCl2 + Cl2↑+ 2H2O中,Mn元素的化合价降低,MnO2为氧化剂,部分Cl元素的化合价升高,则HCl为还原剂,浓盐酸体现了还原性和酸性,由电子守恒可知,氧化剂与还原剂的物质的量比为1:2,
因此,本题正确答案是:还原性;酸性;1:2。


 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应的实验,不能达到实验目的的是
A | B | C | D | |
装置 |
|
|
|
|
实验 | 结合秒表定量比较锌与不同浓度的稀硫酸反应的快慢 | 证明温度对化学平衡的影响 | 验证铁钉发生吸氧腐蚀 | 可证明非金属性Cl>C>Si |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在给定条件下的同分异构体数目正确的是( )
A. C4H10属于烷烃的同分异构体有3种
B. 分子组成是C5H10O2属于羧酸的同分异构体有5种
C. 分子组成是C4H8O属于醛的同分异构体有3种
D. 结构简式为![]() 的一溴代物有5种
的一溴代物有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以苯为基本原料可制备X、Y、Z、W等物质,下列有关说法中正确的是( )
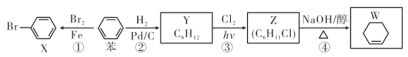
A. 反应①是苯与溴水的取代反应 B. 可用AgN03溶液检测W中是否混有Z
C. X、苯、Y分子中六个碳原子均共平面 D. 反应④中产物除W外还有H2O和NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C、D为短周期元素构成的四种物质,它们有如下转化关系且D为强电解质(其他相关物质可能省略)。下列说法不正确的是( )
![]()
A. 若A为非金属单质,则它与Mg反应的产物中阴、阳离子个数比可能为2∶3
B. 若A为非金属单质,则其组成元素在周期表中的位置可能处于第2周期ⅣA族
C. 不论A为单质还是化合物,D都有可能是同一种物质,该物质的浓溶液在常温下都能使铁和铝发生钝化
D. 若A是共价化合物,0.1molA分子中含有的电子数可能为NA(NA为阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分类是学习和研究化学的一种重要方法,下列物质的分类正确的是( )
A.K2CO3和K2O都属于盐B.KOH和CaCO3都属于碱
C.H2SO4和HNO3都属于酸D.Na2O和Na2SiO3都属于氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
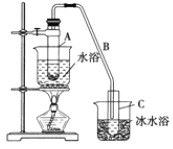
【题目】某化学小组采用类似制乙酸乙酯的装置![]() 如下图
如下图![]() 以环己醇为原料制备环己烯。
以环己醇为原料制备环己烯。
已知: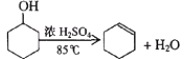
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品将12.5mL环己醇加入试管A中,再加入1 mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是________,导管B除了导气外还具有的作用是_________。
②试管C置于冰水浴中的目的是________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在____层(填“上”或“下”),分液后用________(填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按下图装置蒸馏,冷却水从________口进入。蒸馏时要加入生石灰,目的是__________________________。
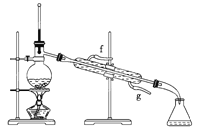
③收集产品时,控制的温度应在______左右,实验制得的环己烯精品质量低于理论产量,可能的原因是______。
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_______。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com