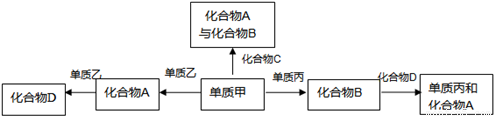
�����û���Ӧ�ĸ��������Ҫע������û���Ӧ�ĸ������ͣ��ס��ҡ�����ǰ������Ԫ�ص����ֵ��ʣ�ӦΪ��������̼�������������������е����֣����ݿ�ͼ��Ҫ����ѡ����ʵ����ʣ����Ͽ�ͼ�ĸ������ʿ����ǣ�AΪ������̼��CO
2����BΪˮ��H
2O����C�ǹ�����õ���Ҫ����ж�CΪC
6H
12O
6��DΪһ����̼��CO��������������O
2��������̼��C��������������H
2����
��1��������A�Ƕ�����̼�����ӵĵ���ʽΪ��
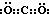
��������CΪ�����ǣ��ṹ��ʽΪ��CH
2OH��CHOH��
4CHO���ʴ�Ϊ��
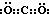
��CH
2OH��CHOH��
4CHO��
��2�������²��1g C��C
6H
12O
6����ȫȼ�տɷų�15.6kJ������1mol��������ȫȼ�շ���Ϊ2808KJ����C��ȫȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��
C
6H
12O
6��s��+6O
2��g���T6CO
2��g��+6H
2O��l������H=-2808 kJ/mol��
�ʴ�Ϊ��C
6H
12O
6��s��+6O
2��g���T6CO
2��g��+6H
2O��l������H=-2808 kJ/mol��
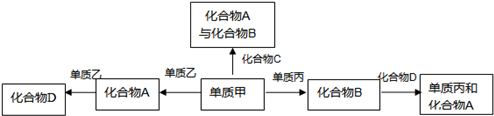
��3��A���������漰�Ļ������У�ˮ��һ�ּ����ĵ���ʣ���A����
B�����ת����ϵ�У���+�ҡ�A��A+�ҡ�D����+����B�������ǻ��Ϸ�Ӧ��ͼ�����ת����ϵ���������ǻ��Ϸ�Ӧ����B��ȷ��
C���������漰�Ļ�����ľ����������ǡ�ˮ��������̼��һ����̼���Ƿ��Ӿ��壬��C��ȷ��
D�����ת����ϵ�У������滯�ϼ۵ı仯����Ϊ������ԭ��Ӧ����D��ȷ��
�ʴ�Ϊ��B��C��D��
��4���üף�O
2��������H
2�����ң�C����������Һ���Թ���һԭ��أ��缫���Ͽ���Ϊʯī�����������������ĵ����������������ӵĵ缫��Ӧ�������Ի����£�����������д��ˮ����ʽ�������ĵ缫��Ӧʽ��O
2+4e
-+4H
+=2H
2O���ʴ�Ϊ��ʯī�� O
2+4e
-+4H
+=2H
2O��
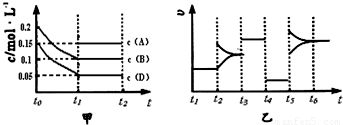
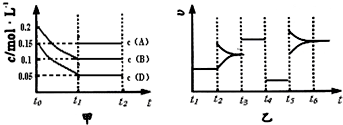
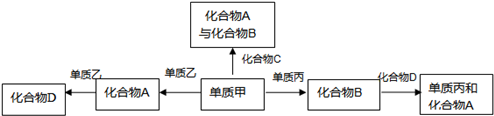
��1������ͼ�������ʼŨ��Ϊ0.2mol/L����BΪH
2O��0.15mol/L����DΪCO��AΪCO
2����� 0.4mol B��0.3mol D��һ������A���������֪�������Ϊ2L��ͼ����B����0.2mol��D����0.2mol��A��ƽ�����ʵ���Ϊ0.3mol����A����ʼ��ΪX�����ݻ�ѧƽ������ʽ��ʽ����õ���
H
2O+CO=CO
2 +H
2��
��ʼ����mol�� 0.4 0.3 X 0
�仯����mol��0.2 0.2 0.2 0.2
ƽ������mol��0.2 0.1 0.3 0.2
��A�����ʵ�����x+0.2=0.3
X=0.1mol
��2��ƽ��Ũ�ȷֱ�Ϊ��C��H
2O ��=0.1mol/L��C��CO��=0.05mol/L��C��CO
2��=0.15mol/L��C��H
2��=0.1mol/L��
K=
=
| 0.1mol/L��0.15mol/L |
| 0.1mol/L��0.05mol/L |
=3
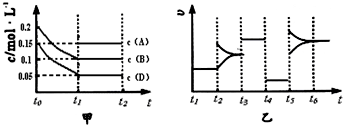
��3��t
4��t
5�θı����������ͼ�����t
4��t
5��ƽ�ⲻ�������ʼ�С�����Ըı�������Ǽ�Сѹǿ��
�ʴ�Ϊ����1��0.1mol ��2��3 ��3����Сѹǿ

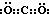
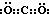






 ��1��A����ʼ���ʵ���Ϊ
��1��A����ʼ���ʵ���Ϊ
 ��1��A����ʼ���ʵ���Ϊ______��
��1��A����ʼ���ʵ���Ϊ______��