
决定化学反应速率的主要因素是 ( )
| A.反应物的浓度 | B.反应温度 |
| C.使用催化剂 | D.反应物的性质 |
科目:高中化学 来源: 题型:单选题
把CoCl2溶解于浓盐酸中,溶液中存在下列平衡:
Co2+ + 4Cl— CoCl4— △H>0
CoCl4— △H>0
粉红色 蓝色
有关上述可逆反应的下列说法不正确的是 ( )
| A.对溶液所在体系加热,溶液蓝色加深 |
| B.对溶液所在体系用冰水降温,上述反应的平衡常数减小 |
| C.室温下,加水稀释,上述反应的平衡常数减小 |
| D.室温下,加水稀释至一定范围,溶液为粉红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将1 mol CO和2 mol H2充入一容积为1L的密闭容器中,分别在250°C、T°C下发生反应:CO(g)+2H2(g)=CH3OH(g),ΔH="a" kJ/mol,如图。下列分析中正确的是
A.250°C时,0?10minH2反应速率为 0.015 mol,/(L.min)
B.平衡时CO的转化率:T℃时小于250℃时
C.其他条件不变,若减小容积体积,CO体积分数增大
D.a<0,平衡常数K:T0C时大于2500C
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在容积为2L的密闭容器中进行反应:CO(g)+2H2(g) CH3OH(g) ,其他条件不变,在300℃和500℃时,甲醇物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是( )
CH3OH(g) ,其他条件不变,在300℃和500℃时,甲醇物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是( )
| A.该反应的△H>0 |
| B.其他条件不变,升高温度反应的平衡常数增大 |
C.300℃时,0-t 1min内 CH3OH的平均生成速率为 mol·L-1 min-1 mol·L-1 min-1 |
D.A点的反应体系从300℃升高到500℃,达到平衡时 减小 减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
2 mol A与2 mol B混合于2 L的密闭容器中,发生如下反应:2A(g)+3B(g) 2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
2C(g)+zD(g),若2 s后,A的转化率为50%,测得v(D)=0.25 mol·L-1·s-1,下列推断正确的是( )
A.v(C)=0.2 mol·L-1·s-1 B.z=3
C.B的转化率为25% D.C的体积分数为28.6%
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列措施中,能减慢化学反应速率的是
| A.食物储存在冰箱里 |
| B.将块状固体药品研细后再反应 |
| C.用MnO2作H2O2分解反应的催化剂 |
| D.用30%H2SO4溶液代替5%H2SO4溶液与锌粒反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对化学反应限度的叙述,错误的是
| A.任何可逆反应都有一定的限度 |
| B.化学反应达到限度时,正逆反应速率相等 |
| C.化学反应的限度与时间的长短无关 |
| D.化学反应的限度是不可改变的 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述中可以说明反应2HI(g)  H2(g)+I2(g)已达平衡状态的是
H2(g)+I2(g)已达平衡状态的是
①单位时间内生成n mol H2的同时生成n mol HI ②一个H—H键断裂的同时有两个H—I键断裂 ③百分组成HI%=I2% ④反应速率v(H2)=v(I2)=1/2v(HI) ⑤[HI]∶[H2]∶[I2]=2∶1∶1 ⑥v(HI)分解=v(HI)生成 ⑦压强不变
| A.①③⑤ | B.②⑥ | C.④⑤ | D.④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对下列图像的描述正确的是( )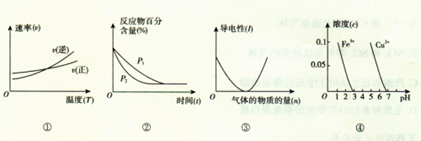
A.根据图①可判断反应A2(g)+3B2(g)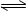 2AB3(g)的△H>0 2AB3(g)的△H>0 |
B.图②可表示压强(P)对反应2A(g)+2B(g)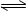 3C(g)+D(s)的影响 3C(g)+D(s)的影响 |
| C.图③可表示向醋酸溶液通人氨气时,溶液导电性随氨气量的变化 |
| D.根据图④,除去CuSO4溶液中的Fe3+,可加入CuO调节pH至3~5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com