
���ݻ�Ϊ2L���ܱ������н��з�Ӧ��CO(g)+2H2(g) CH3OH(g) �������������䣬��300���500��ʱ���״����ʵ���n(CH3OH)-��Ӧʱ��t�ı仯������ͼ��ʾ������˵����ȷ���ǣ� ��
CH3OH(g) �������������䣬��300���500��ʱ���״����ʵ���n(CH3OH)-��Ӧʱ��t�ı仯������ͼ��ʾ������˵����ȷ���ǣ� ��
| A���÷�Ӧ�ġ�H��0 |
| B�������������䣬�����¶ȷ�Ӧ��ƽ�ⳣ������ |
C��300��ʱ��0-t 1min�� CH3OH��ƽ����������Ϊ mol��L��1 min��1 mol��L��1 min��1 |
D��A��ķ�Ӧ��ϵ��300�����ߵ�500�棬�ﵽƽ��ʱ ��С ��С |
C
�������������A����ͼ���֪���¶�Խ�ߣ�����ƽ��ʱ�״������ʵ���ԽС����˵�������¶�ƽ�����淴Ӧ�ƶ������Ը÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ������H��0����A����B����ͼ���֪���¶�Խ�ߣ�����ƽ��ʱ�״������ʵ���ԽС�������¶�ƽ�����淴Ӧ�ƶ���ƽ�ⳣ����С����B����C��ƽ��ʱ�״������ʵ���Ϊn1mol���״���Ũ����n1mol��2L��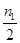 mol/L�����Լ״���ʾ�ķ�Ӧ�����Ǧԣ�CH3OH����
mol/L�����Լ״���ʾ�ķ�Ӧ�����Ǧԣ�CH3OH���� mol��L��1 min��1������ѡ��C��ȷ��D��A��ķ�Ӧ��ϵ��300�����ߵ�500�棬ƽ�����淴Ӧ���״������ʵ�����С�����������ʵ������ʴﵽƽ��ʱ
mol��L��1 min��1������ѡ��C��ȷ��D��A��ķ�Ӧ��ϵ��300�����ߵ�500�棬ƽ�����淴Ӧ���״������ʵ�����С�����������ʵ������ʴﵽƽ��ʱ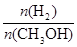 �������ѡ��D����ȷ����ѡC��
�������ѡ��D����ȷ����ѡC��
���飺�������������ƽ��״̬��ƽ�ⳣ����Ӱ���Լ���Ӧ���ʵļ����ͼ��ʶ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ���¶��µ��ܱ������з�����Ӧ��X(g)��3Y(g) 2Z(g) ��H��
2Z(g) ��H�� ����ͼ�Ƿ�Ӧ��ƽ�⼰�ı�����ƽ���ƶ���ͼ������˵���������
����ͼ�Ƿ�Ӧ��ƽ�⼰�ı�����ƽ���ƶ���ͼ������˵���������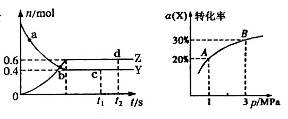
A.c���d��X�����淴Ӧ�������
B.��ʼʱ������Y�����ʵ���Ϊ1.3mol
C.ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ����K(A)��K(B)
D.ƽ��״̬��A�䵽Bʱ���ų���������Q(A)��Q(B)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
ij�¶������ݻ�������ܱ������У�����aX��g��+bY��g�� cW��g����Ӧ��������1 mol X��lmol Y���ﵽƽ��ʱ��W��Ũ��Ϊ0��2 mol/L������˵���������
cW��g����Ӧ��������1 mol X��lmol Y���ﵽƽ��ʱ��W��Ũ��Ϊ0��2 mol/L������˵���������
| A���ﵽƽ��ʱ������b mol Y��ͬʱ����c moI W |
| B���������¶ȣ�W�����ʵ���Ũ�ȼ�С����÷�Ӧ��H<0 |
| C������ʼͶ��X��Y�����ʵ����ֱ�Ϊamol��bmol����ƽ��ʱX��Y��ת������� |
| D������ͬ�����£��ٳ���l mol X��1 mol Y������ƽ��ʱ��W��Ũ��Ϊ0��4 mol/L����a+b>c |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ�������£��̶��ݻ����ܱ������з�Ӧ��2NO2(g) 2NO (g) +O2 (g) ��H��0���ﵽƽ�⡣���ı�����һ������X��Y��X�ı仯����ͼ�����ߵ���
2NO (g) +O2 (g) ��H��0���ﵽƽ�⡣���ı�����һ������X��Y��X�ı仯����ͼ�����ߵ���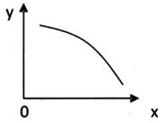
| A����X��ʾ�¶�ʱ��Y��ʾNO2�����ʵ��� |
| B����X��ʾѹǿʱ��Y��ʾNO2��ת���� |
| C����X��ʾ��Ӧʱ��ʱ��Y��ʾ���������ܶ� |
| D����X��ʾNO2�����ʵ���ʱ��Y��ʾO2�����ʵ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ�ܱ������з�����Ӧ��2X(g)��Y(g) aZ(g) ��H=QkJ��mol-1����ʼ�������2:1��X��Y���뷴Ӧ���У�һ�������·�����Ӧ��ͼ��ͼ���Ǹ��ݷ�Ӧ���Ƶ�ͼ�������й�˵����ȷ����
aZ(g) ��H=QkJ��mol-1����ʼ�������2:1��X��Y���뷴Ӧ���У�һ�������·�����Ӧ��ͼ��ͼ���Ǹ��ݷ�Ӧ���Ƶ�ͼ�������й�˵����ȷ����
| A��ͼ�ף�P1��P2��a �� 3 |
| B��ͼ�ף�T1��T2��Q��0 |
| C��ͼ�ң�t1ʱ��ʾ���¡���ѹ�����£���ƽ����ϵ�г���һ������Z���� |
| D��ͼ�ң����a=3, t2ʱ��ʾ����ϵ�м����˴��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��ӦA��g��+3B��g��  2C��g��+D��g������ij��ʱ���ڣ���A��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ2 mol/��L��s��������C��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ
2C��g��+D��g������ij��ʱ���ڣ���A��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ2 mol/��L��s��������C��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ
| A��1 mol/��L��s�� | B��3 mol/��L��s�� |
| C��4 tool/��L��s�� | D��2 mol/��L��s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
������ѧ��Ӧ���ʵ���Ҫ������ �� ��
| A����Ӧ���Ũ�� | B����Ӧ�¶� |
| C��ʹ�ô��� | D����Ӧ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ���¶��£���������˵�����淴ӦA��g��+2B(g)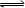
 2C(g) �ﵽƽ��ģ� ��
2C(g) �ﵽƽ��ģ� ��
A��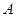 �� ��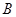 �� ��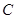 ��Ũ��֮��Ϊ1:2:2 ��Ũ��֮��Ϊ1:2:2 |
B����λʱ��������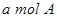 ��ͬʱ����2a mol C ��ͬʱ����2a mol C |
C��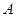 ��Ũ�Ȳ��ٱ仯 ��Ũ�Ȳ��ٱ仯 |
| D��������������ʵ���Ϊ2a mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ͬ�¶��£������Ϊ0.25 L�����������ܱ������з������淴Ӧ��N2(g)��3H2(g) 2NH3(g) ��H����92.6kJ/moL��ʵ������ʼ��ƽ��ʱ���й��������±���
2NH3(g) ��H����92.6kJ/moL��ʵ������ʼ��ƽ��ʱ���й��������±���
| ������� | ��ʼʱ���������ʵ���/mol | ��ƽ��ʱ��ϵ �����ı仯 | ||
| N2 | H2 | NH3 | | |
| | 1 | 3 | 0 | �ų�������23.15kJ |
| �� | 0.9 | 2.7 | 0.2 | �ų�������Q |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com