
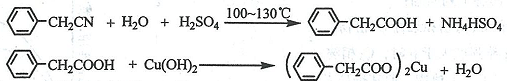
���� ��1�����ƴ�����ʱ��Ӧ���ܶȴ��ע���ܶ�С��Һ���У���ֹ���ʱ�ų���ʹҺ�ηɽ���
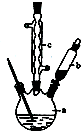
��2����ͼ��֪������b�ɼ��뷴ӦҺ��cΪ�����ܣ�ʹ������Һ����������������b�ɼ��뷴ӦҺ����Ӧ�������������ˮ�������¶ȣ���С��������ܽ�ȣ����뱽�����Ʒ�����ù��˲�����
��3��������������ˮ����ˮ�е��ܽ�Ƚ�С���ɷ�Ӧ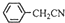 +H2O+H2SO4 $\stackrel{100��130��}{��}$
+H2O+H2SO4 $\stackrel{100��130��}{��}$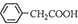 +NH4HSO4��֪��40g���������ɱ�����Ϊ40g��$\frac{136}{117}$=46.5g��
+NH4HSO4��֪��40g���������ɱ�����Ϊ40g��$\frac{136}{117}$=46.5g��
��4��������ˮϴ�ӳ�������������ϴ�Ӹɾ�����������������ϴ��Һȷ���Ƿ�ϴ�Ӹɾ���
��5��������������ˮ�������Ҵ�������ܼ����Ҵ�������������ܽ�ȣ�
��6����ƿ������ѹǿ̫��
��� �⣺��1��ϡ��Ũ����ų��������ȣ����ƴ�����ʱ��Ӧ���ܶȴ��ע���ܶ�С��Һ���У���ֹ���ʱ�ų���ʹҺ�ηɽ������������ˮ��Ũ������Ⱥ�˳�����ȼ�ˮ���ټ���Ũ���ᣬ
�ʴ�Ϊ���ȼ�ˮ���ټ���Ũ���
��2����ͼ��֪������b�ɼ��뷴ӦҺ��Ϊ��Һ©����cΪ���������ܣ�������Ϊ��������ʹ�����ķ�ӦҺ������������b������Ϊ�μӱ����棻��Ӧ�������������ˮ�������¶ȣ���С��������ܽ�ȣ��������ˮ�ɱ��ڱ��������������뱽�����Ʒ�����ù��˲���������Ҫ������Ϊ©�����ձ�����������
�ʴ�Ϊ��������������ʹ�����ķ�ӦҺ����������Һ©�����μӱ����棻 ���ڱ�����������BCE��
��3��������������ˮ����ˮ�е��ܽ�Ƚ�С�����ᴿ������ķ������ؽᾧ���ɷ�Ӧ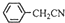 +H2O+H2SO4 $\stackrel{100��130��}{��}$
+H2O+H2SO4 $\stackrel{100��130��}{��}$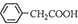 +NH4HSO4��֪��40g���������ɱ�����Ϊ40g��$\frac{136}{117}$=46.5g�����յõ�44g��Ʒ��������IJ�����$\frac{44g}{46.5g}$��100%=95%��
+NH4HSO4��֪��40g���������ɱ�����Ϊ40g��$\frac{136}{117}$=46.5g�����յõ�44g��Ʒ��������IJ�����$\frac{44g}{46.5g}$��100%=95%��
�ʴ�Ϊ���ؽᾧ��95%��
��4��������ˮϴ�ӳ�������������ϴ�Ӹɾ�����������������ϴ��Һȷ���Ƿ�ϴ�Ӹɾ��������ϴ�ɾ���ʵ�������������ȡ���һ������ϴ��Һ������ϡ���ᣬ�ټ���AgNO3��Һ���ް�ɫ���dz��֣�
�ʴ�Ϊ��ȡ�������һ��ϴ��Һ������ϡ���ᣬ�ټ�AgNO3��Һ���ް�ɫ���dz��֣�
��5��������������ˮ�������Ҵ�������ܼ����Ҵ�������������ܽ�ȣ�Ȼ����Cu��OH��2��Ӧ��ȥ�����ᣬ������ܼ����Ҵ������������������ܽ�ȣ����ڳ�ַ�Ӧ��
�ʴ�Ϊ�����������ܽ�ȣ����ڳ�ַ�Ӧ��
��6����ƿ������ѹǿ̫�ɸ�Ϊ��ѹ��Һ©����ʹ����ѹǿ��ȣ��ʴ�Ϊ����ѹ��Һ©����
���� ���⿼�鱽����ͭ�ĺϳɣ����������Ʊ�ʵ�鼰�л������ʵĿ��飬���պϳɷ�Ӧ��ʵ��װ�õ�����Ϊ���Ĺؼ����ۺϿ���ѧ��ʵ�鼼�ܺͷ�������������������Ŀ�Ѷ��еȣ�ע����Ϣ�Ĵ�����Ӧ�ã���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | c��NH4+��=c��Cl-����NH4Cl�Ͱ�ˮ�Ļ����Һ | |
| B�� | c��H+��=1.0��10-7mol•L-1����Һ | |
| C�� | pH=7����Һ | |
| D�� | �����½�pH=3������pH=11�ļ�������Ϻ����Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
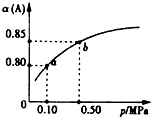 һ���¶��£����ݻ�Ϊ1L���ܱ������м���0.5molA��0.25molB��������Ӧ��2A��g��+B��g��?2C���������ﵽƽ��ʱ���ų�����Q1kJ�������¶Ȳ��䣬A��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ��������˵����ȷ���ǣ�������
һ���¶��£����ݻ�Ϊ1L���ܱ������м���0.5molA��0.25molB��������Ӧ��2A��g��+B��g��?2C���������ﵽƽ��ʱ���ų�����Q1kJ�������¶Ȳ��䣬A��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ��������˵����ȷ���ǣ�������| A�� | ��������������ܶȱ��ֲ��䣬˵����Ӧһ���ﵽƽ��״̬ | |
| B�� | ������ͬ�����£���Ϊֻ����0.5 mol C����Ӧ�ﵽƽ�ⷴ���ų�����Q1kJ | |
| C�� | ƽ��״̬��a�䵽bʱ����ѧƽ�ⳣ��K��a��=K��b�� | |
| D�� | ��ͼ���֪������Cһ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
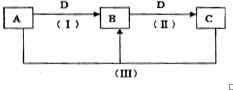 A��B��C��D������ѧ��ѧ�г������ʣ�����A��B��C������ͬһ��Ԫ�أ���һ���������ת����ϵ���£����ַ�Ӧ�е�ˮ����ȥ������������ش��������⣺
A��B��C��D������ѧ��ѧ�г������ʣ�����A��B��C������ͬһ��Ԫ�أ���һ���������ת����ϵ���£����ַ�Ӧ�е�ˮ����ȥ������������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ���и���֮��Ĵ�����ϵ��ȷ���ǣ�������
���и���֮��Ĵ�����ϵ��ȷ���ǣ�������| ѡ�� | A | B | C | D |
| �� | ���� | ���������� | �Ͻ� | ͭ�� |
| �� | �� | ���������� | ����� | �� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֪ H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ•mol-1���� H2SO4��Ba��OH��2��Ӧ�ķ�Ӧ�ȡ�H=2����-57.3��kJ•mol-1 | |
| B�� | �����ǵ�ȼ������2800 kJ•mol-1���� $\frac{1}{2}$C6H12O6��s��+3O2��g���T3CO2��g��+3H2O��l����H=-1400kJ•mol-1 | |
| C�� | H2��g����ȼ������285.8 kJ•mol-1���� 2H2O��g���T2H2��g��+O2��g����H=+571.6 kJ•mol-1 | |
| D�� | ȼ�ϵ���н��״�����ת��Ϊ�������Ȼ�ѧ����ʽ�� CH3OH��g��+$\frac{1}{2}$O2��g���TCO2��g��+2H2��g����H=-192.9 kJ•mol-1���� CH3OH��g����ȼ����Ϊ 192.9 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ձ� | B�� | ������ | C�� | ����ƿ | D�� | ��Һ©�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com