
【题目】下列有关实验的推理正确的是
A.向CuSO4·5H2O晶体中滴加浓硫酸,晶体表面变为白色,说明浓硫酸具有强氧化性
B.向溶液X中滴加BaCl2溶液,有白色沉淀生成,说明溶液X中含![]()
C.向品红溶液中通入气体Y,溶液变为无色,加热后变红,说明Y为SO2
D.向溶液Z中通入Cl2,再滴加KSCN溶液后变红,说明溶液Z中含Fe3+
【答案】C
【解析】
A.向CuSO4·5H2O晶体中滴加浓硫酸,由于浓硫酸吸收了CuSO4·5H2O中的结晶水从而使晶体表面变为白色,说明浓硫酸具有吸水性,A错误;
B.向溶液X中滴加BaCl2溶液,有白色沉淀生成,溶液X中不一定含有![]() ,可能含有Ag+或
,可能含有Ag+或![]() 、
、![]() 等,检验
等,检验![]() 必须先向溶液中加入足量稀盐酸,无明显现象,再加入BaCl2溶液,若有白色沉淀生成说明含
必须先向溶液中加入足量稀盐酸,无明显现象,再加入BaCl2溶液,若有白色沉淀生成说明含![]() ,B错误;
,B错误;
C.向品红溶液中通入气体Y,溶液变为无色,该气体可能为SO2、Cl2等,加热后变红,说明该气体漂白后的无色物质不稳定、容易分解,则该气体Y为SO2,C正确;
D.向溶液Z中通入Cl2,再滴加KSCN溶液后变红,说明通入Cl2后的溶液中含Fe3+,溶液Z中不一定含Fe3+,溶液Z中只含Fe2+、不含Fe3+时也会产生相同的实验现象,D错误;
答案选C。


科目:高中化学 来源: 题型:
【题目】在一定温度下的某恒容密闭容器中,建立下列化学平衡:C(s)+H2O(g)CO(g)+H2(g)。在一定条件下不能表示该可逆反应已达到化学平衡状态的是( )
A.体系压强不再发生变化
B.v正(CO)=v逆(H2O)
C.体系的气体的密度不再变化
D.1 mol HH 键断裂的同时形成 2 mol HO 键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有0.2mol某有机物和0.5mol氧气在一密闭容器中燃烧得产物为CO2、CO、H2O(气)。产物通过浓硫酸时,浓硫酸的质量增加了7.2g;再通过灼热的氧化铜时,氧化铜的质量减少了3.2g;又通过碱石灰时,碱石灰的质量增加了17.6g。该有机物的化学式是( )
A.C2H4B.C2H6OC.C2H6O2D.C3H6O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某Na2CO3、NaAlO2的混合溶液中逐滴加入1molL1的盐酸,测得溶液中的CO32、HCO3、AlO2、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示。则下列说法正确的是( )(已知:H2CO3的电离平衡常数K1 = 4.3×107,K2 = 5.6×1011;Al(OH)3的酸式电离平衡常数K=6.3×1013)

A. a曲线表示的离子方程式为:AlO2+4H+ = Al3+ + 2H2O
B. M点时生成的CO2为0.05 mol
C. 原混合溶液中的CO32与AlO2的物质的量之比为1:2
D. V1:V2=1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为:PbSO4+2LiCl+Ca = CaCl2+Li2SO4+Pb。下列有关说法正确的是

A. 正极反应式:Ca + 2Cl--2e- = CaCl2
B. 放电过程中,Li+向负极移动
C. 没转移0.1mol电子,理论上生成20.7 g Pb
D. 常温时,在正负极间接上电流表或检流计,指针不偏转
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请运用原电池原理设计实验,验证 Cu2+、Fe3+氧化性的强弱。请写出电极反应式。
(1)负极 __________________________
(2)正极 __________________________________
(3)并在方框内画出实验装置图,要求用烧杯和盐桥,并标出外电路中电子流向。________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁、戊五种物质是中学化学常见的物质,其中甲、乙均为单质,它们的转化关系如图所示![]() 某些条件和部分产物已略去
某些条件和部分产物已略去![]() 。下列说法正确的是
。下列说法正确的是
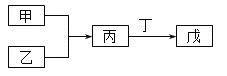
A.若甲可以与NaOH溶液反应放出H2,则丙一定是两性氧化物
B.若甲为短周期中最活泼的金属,且戊为碱,则丙生成戊一定是氧化还原反应
C.若丙、丁混合产生大量白烟,则乙可能具有漂白性
D.若甲、丙、戊都含有同一种元素,则三种物质中,该元素的化合价由低到高的顺序可能为甲![]() 丙
丙![]() 戊
戊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组拟探究CO2和锌粒反应是否生成CO,已知CO能与银氨溶液反应产生黑色固体。实验装置如图所示:

下列说法正确的是
A. 实验开始时,先点燃酒精灯,后打开活塞K
B. b、c、f中试剂依次为氢氧化钠溶液、浓硫酸、银氨溶液
C. 装置e的作用是收集一氧化碳气体
D. 用上述装置(另择试剂)可以制备氢气并探究其还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如下图所示。下列说法错误的是
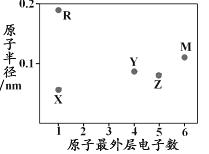
A. R的氧化物含有离子键 B. 最高价含氧酸的酸性:Z<Y
C. M的氢化物常温常压下为气体 D. Y形成的化合物种类最多
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com