
下列实验装置能达到实验目的是
 |
A、比较碳酸钠和碳酸氢钠热稳定性大小
B、用铜和稀硝酸制取并收集少量NO
C、验证氨气在水中溶解性
D、实验室用氯化铵制氨气
科目:高中化学 来源: 题型:
下列说法中正确的是( )
A.乙烯中C=C的键能是乙烷中C—C的键能的2倍
B.同一原子中,2p,3p,4p能级的轨道依次增多
C. C—O键的极性比N—O键的极性大
D.NH4+中4个N—H键的键能不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
硝酸是极其重要的化工原料,工业上将产生的NO2在密闭容器中用水多次反复循环吸收制备硝酸。
(1)工业上用水吸收NO2生产HNO3,生成的气体经多次氧化、吸收的循环操作充分转化为硝酸(假定上述过程无其他损失)。试写出上述反应的化学方程式:
_________________________________________________________________
___________________________________ _____________________________________。
_____________________________________。
(2)为了证明NO也可以与氧气和水共同反应生成HNO3,某学生设计了如图所示装置(有关夹持装置已略去)。
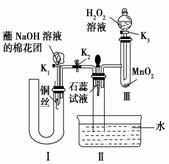
①检查装置气密性良好后,为观察到NO气体生成,打开K1,关闭K2,应从U形管的长管口注入稀硝酸至________后,迅速关闭K1,观察到U形管内的现象是____________
________________________________________________________________________。
②装置Ⅲ中发生反应的化学方程式为________________________________。
③蘸NaOH溶液的棉花团的作用是________________________________________。
④打开K2,至装置Ⅱ中长玻璃管中的气体呈无色后,打开K3,反应一段时间后,长玻璃管中并 未充满液体。设计简单方法检验长玻璃管中的气体是否含NO_____________
未充满液体。设计简单方法检验长玻璃管中的气体是否含NO_____________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在伪劣美白化妆品中常添加双氧水起到快速美白的效果,使用时间长了会对皮肤造成强烈刺激,严重的可能烧坏表皮层,让皮肤变粗糙、长疱。可采用高锰酸钾溶液检验化妆品中是否含有双氧水,该反应的方程式为:2KMnO4+3H2O2→ 2MnO2+2KOH + 3O2↑+ 2H2O,下列有关说法正确的是:
A、1mol 的高锰酸钾参与反应有6 mol电子发生转移
B、高锰酸钾与双氧水都是常见氧化剂,高锰酸钾的氧化性比双氧水弱
C、上反应中双氧水做还原剂
D、在高锰酸钾溶液中加入足量含有双氧水的化妆品样品,溶液也不会褪色。
查看答案和解析>>
科目:高中化学 来源: 题型:
水是一种宝贵的自然资源。
(1)生活污水中,常含N、P化合物而造成水体植物富营养化污染。水中的氨在微生物的作用下,可发生以下一系列变化:A、 NH3 + O2 →HNO2+ H2O(未配平)
B、2HNO2+O2 → 2HNO3,回答以下问题
① 配平反应A并标出电子转移的方向与数目:
____NH3+ ___O2 → ___HNO2+ ____ H2O
② 反应B中被氧化的元素是 。
(2)氧化还原法是处理污水常用的方法之一。某工厂排放的污水,经检测,污水中含有
0.012 mol/L的游离态溴,可用Na2SO3还原除去污水中的溴,请写出其离子方程式:
若处理5L这种污水,至少需加入0.05mol/L的Na2SO3溶液 L才能将单质溴全部除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
某小组同学查到一份研究过氧化氢溶液与氢碘酸(HI)反应的实验资料,具体如下:
资料1:室温下,过氧化氢溶液可与氢碘酸(HI)反应,溶液为棕黄色。
资料2:实验数据如下表所示。
| 实验编号 | 1 | 2 | 3 | 4 | 5 |
| 实验条件 | 保持25℃,101kP条件下 | ||||
| c(H2O2) | 0.1 | 0.1 | 0.1 | 0.3 | 0.3 |
| c(HI) | 0.1 | 0.2 | 0.3 | 0.1 | 0.1 |
| 出现棕黄色时间/s | 13.1 | 6.5 | 4.3 | 4.4 | 4.4 |
(1) 过氧化氢溶液与氢碘酸(HI)反应的化学方程式为 。
(2)①观察资料2中实验编号为1-3数据,分析解释出现棕黄色由慢变快的原因是 。
②该组同学对编号4、5的实验分别升高不同温度,发现升高温度较小的一组,棕黄色出现加快,升高温度较大的一组,棕黄色出现反而变慢,
请你给与分析解释 。
(3)该小组同学欲用碘化钾替代氢碘酸验证上述实验。在实验过程中,未观察到溶液变为棕黄色,却观察到产生无色气体。于是,该小组同学提出假设:KI可能是过氧化氢分
解反应的催化剂(实验室提供KI溶液),并设计如下实验验证其假设。
实验步骤:
I. 取2支试管,向试管1中加入2 mL 0.1 mol/L H2O2溶液,向试管2中加入…….。
II. ……。
III.分别将2支试管置于40℃水浴中。
①补全实验步骤
I: 。
II: 。
②实验现象证明该小组同学假设成立,该实验现象是 。
(4)实验后,该小组同学进一步查阅资料,发现了如下图所示的数据关系,并根
据该数据图提出了如下新假设: 。
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
两种气态烃的混合气体0.1mol,完全燃烧得0.16molCO2和3.6g水,下列说法正确的是
A.混合气体中一定有甲烷 B.混合气体中一定是甲烷和乙烯
C.混合气体中一定有乙烷 D.混合气体中一定有乙炔(CH≡CH)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com