
【题目】用![]() 表示阿伏加德罗常数的数值,下列说法中正确的是
表示阿伏加德罗常数的数值,下列说法中正确的是
A. 在常温常压下,11.2L氯气所含的原子数为![]()
B. 2.3g金属钠被氧化成Na2O2,转移电子数为0.1![]()
C. 5.6g铁与足量稀盐酸反应转移的电子数为0.3![]()
D. 2L 0.1 mol/LNa2SO4溶液中含有的Na+的数为0.2![]()
科目:高中化学 来源: 题型:
【题目】(1)给定条件下的下列四种物质:①标准状况下112mL液态水,②含有40mol质子的NH3, ③2mol的乙醇,④4g氦气,则上述物质中所含分子数目由多到少的顺序是________________(填序号)。
(2)标准状况下,0.51g某气体的体积为672mL,则该气体相对分子质量为______。
(3)将100mLH2SO4和HCl混合溶液分成两等份,一份中加入含0.2molNaOH溶液时恰好中和完全,向另一份中加入含0.05molBaCl2溶液时恰好沉淀完全,则原溶液中c(Cl-)=_________。
(4)标准状况下,VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液密度为ρg/mL,则所得溶液溶质物质的量浓度=________________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
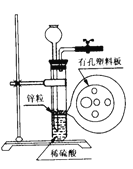
【题目】右图为实验室制氢气的简易装置。若在加稀硫酸时,发现锌粒与稀硫酸没有接触而稀硫酸又不够了,为使反应顺利进行,则可以从长颈漏斗中加入的试剂是 ( )
①食盐水②KNO3溶液③适量硫酸铜溶液④Na2CO3溶液⑤CCl4 ⑥浓氨水
A. ①②④ B. ②⑥ C. ②③⑤ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废水脱氮工艺中有一种方法是在废水中加入过量NaClO使NH4+完全转化为N2,该反应可表示为2NH4++3ClO-=N2↑+3Cl-+2H++3H2O。下列说法中,不正确的是
A. 反应中氮元素被氧化,氯元素被还原
B. 还原性NH4+< Cl-
C. 反应中每生成1 mol N2,转移6 mol电子
D. 经此法处理过的废水不可以直接排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将溶质的质量分数为a%、物质的量浓度为c1mol/L的稀硫酸加热蒸发掉一定量的水,使质量分数为2a%,此时硫酸的物质的量浓度为c2 mol/L.已知硫酸浓度越大,密度越大,则c1 与c2的数值关系是( )
A.c1=2c2
B.c2=2cl
C.c2>2c1
D.c2<2cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化合物分子的核磁共振氢谱中氢原子的吸收峰只有一种的是( )
A.CH3OCH3
B.CH3CH2OH
C.CH3CH2CH3
D.CH3COCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有短周期X、Y、Z、M、W为五种短周期元素.其中X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L﹣1;W的质子数是X、Y、Z、M四种元素质子数之和的一半.下列说法正确的是( )
A.原素Z,W的简单离子的电子层结构不同
B.Y的最高价氧化物的水化物能与其简单气态氢化物反应生成盐且显碱性
C.由X元素形成的单质不一定是原子晶体
D.由X,YCZ,M四种元素形成的化合物一定既有离子键,又有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
(1)氯气与氢氧化钠在70℃时反应,生成物中NaClO3和NaClO的物质的量之比为3:1的离子方程式_____________________________________________。
(2)工业上可用KClO3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之比为____。
(3)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银
①H3PO2中,P元素的化合价为_______。
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4 :1,则氧化产物为____(填化学式)。
(4)取300mL 0.2mol/L 的KI溶液与一定量的酸性KMnO4 溶液恰好反应,生成等物质的量的I2和KIO3,则消耗KMnO4的物质的量的是__________mol。
(5)在Fe(NO3)3溶液中加入Na2SO3溶液,溶液先由棕黄色变为浅绿色,过一会又变为棕黄色,溶液先变为浅绿色的离子方程式是_______________,又变为棕黄色的原因是_________(用离子方程式解释)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com