
科目:高中化学 来源:2015-2016学年吉林实验中学高一上学期期中考试化学试卷(解析版) 题型:选择题
下列离子方程式中,只能表示一个化学反应的是( )
①CO32-+2H+===CO2↑+H2O
②Ba2++2OH-+2H++SO42-===BaSO4↓+2H2O
③Ag++Cl-===AgCl↓
④Fe+Cu2+===Fe2++Cu
⑤Cl2+H2O===H++Cl-+HClO
A.①③ B.②④ C.②⑤ D.只有⑤
查看答案和解析>>
科目:高中化学 来源:2016届山东省济宁市高三上学期期中考试化学试卷(解析版) 题型:选择题
在一定浓度的浓硝酸中加入m克铜镁合金恰好完全溶解(假定硝酸的还原产物只有NO2),向反应后的混合溶液中滴加bmol/LNaOH溶液,当滴加到 v mL时,恰好完全反应,得到沉淀质量为n 克,则下列有关该实验的说法中正确的有( )
①沉淀中氢氧根的质量为(n-m)克 ②恰好溶解后溶液中的NO3-离子的物质的量为bv mol
③反应过程中转移的电子数为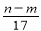 mol ④生成NO2气体的体积为
mol ④生成NO2气体的体积为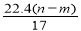 L
L
⑤与合金反应反应的硝酸的物质的量为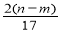 mol
mol
A.①②③④⑤ B. ①③④⑤ C. ①③⑤ D. ①②③⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州十校联合体高二上学期期中测试化学试卷(解析版) 题型:简答题
工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如下图:

(1)此流程的第II步反应为:CO(g)+H2O(g)  H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
温度/℃ | 400 | 500 | 830 |
平衡常数K | 10 | 9 | 1 |
从上表可以推断:此反应是 (填“吸”或“放”)热反应。在830℃下,若开始时向恒容密闭容器中充入1mo1CO和2mo1H2O,则达到平衡后CO的转化率为 。
(2)在500℃,按照下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第II步反应,达到平衡后下列关系正确的是 。
实验编号 | 反应物投入量 | 平衡时H2浓度 | 吸收或放出的热量 | 反应物转化率 |
A | 1、1、0、0 | c1 | Q1 | α1 |
B | 0、0、2、2 | c2 | Q2 | α2 |
C | 2、2、0、0 | c3 | Q3 | α3 |
A.2c1= c2 =c3 B.2Q1=Q2=Q3 C.α1 =α2 =α3 D.α1 +α2 =1
(3)在一个绝热等容容器中,不能判断此流程的第II步反应达到平衡的是 。
①v(CO2)正=v(H2O)逆
②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化
(4)下图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件使浓度发生变化的情况:图中t2时刻发生改变的条件是 、 (写出两种)。
若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变)。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省温州十校联合体高一上学期期中测试化学试卷(解析版) 题型:填空题
用双线桥表示下列反应的电子转移方向和数目,并回答下列问题:
3I2 + 6NaOH = 5NaI + NaIO3 + 3H2O
(1) 是氧化剂, 是还原剂,氧化产物是 ;
(2)氧化剂与还原剂的物质的量之比为 ,当反应消耗3mol NaOH时,转移的电子数目为 。
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期期中联考化学试卷(解析版) 题型:选择题
下列有关Fe2(SO4)3溶液的叙述正确的是
A.该溶液中K+、Fe2+、SCN-、Br-可以大量存在
B.和KI溶液反应的离子方程式: Fe3++2I-=Fe2++I2
C.和Ba(OH)2溶液反应离子方程式:Fe3++ SO42-+Ba2++3OH-=Fe(OH)3↓+BaSO4↓
D.1 L0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2g Fe
查看答案和解析>>
科目:高中化学 来源:2016届湖南省澧县、桃源、益阳三校高三上学期联考化学试卷(解析版) 题型:选择题
下列比较、归纳一定正确的是
A.酸性:HClO4>H2CO3>H2SiO3
B.稳定性:HF<H2O<NH3
C.离子半径:Na+>F-> Al3+
D.沸点:HI>HBr>HF
查看答案和解析>>
科目:高中化学 来源:2016届辽宁师范大学附属中学高三上学期期中考试化学试卷(解析版) 题型:选择题
下列叙述正确的是( )
A.中和热测定实验用的小烧杯和物质的量浓度溶液配制用的容量瓶都必须干燥
B.用已知浓度的盐酸滴定未知浓度的氢氧化钠溶液终点时仰视读数,氢氧化钠浓度偏低
C.配制2.0 mol·L-1的硫酸,若定容时俯视,则所得溶液浓度偏高(其他操作均正确)
D.用铜电极电解2.0 mol·L-1的硫酸,阴阳两极生成气体的体积之比为2∶1
查看答案和解析>>
科目:高中化学 来源:2016届贵州遵义航天高中高三上学期第三次模拟理综化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数的值。下列叙述正确的是
A. 常温下,44g CO2中含有2NA个碳氧双键
B. 标准状况下,0.1mol Al3+含有的核外电子数为0.3NA
C. 室温下,1L pH=13的氢氧化钡溶液所含氢氧根离子数为0.2NA
D. 将1mol N2和3mol H2通入密闭容器中,在一定条件下充分反应,转移电子数为6NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com