
NA为阿伏加德罗常数的值。下列叙述正确的是
A. 常温下,44g CO2中含有2NA个碳氧双键
B. 标准状况下,0.1mol Al3+含有的核外电子数为0.3NA
C. 室温下,1L pH=13的氢氧化钡溶液所含氢氧根离子数为0.2NA
D. 将1mol N2和3mol H2通入密闭容器中,在一定条件下充分反应,转移电子数为6NA
科目:高中化学 来源:2015-2016学年浙江省温州十校联合体高一上学期期中测试化学试卷(解析版) 题型:选择题
若你家的花生油不小心混入大量水,利用你所学的知识,最简便的分离方法是
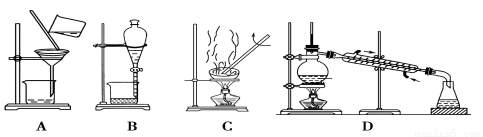
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第三次考试化学试卷(解析版) 题型:选择题
下列反应方程式不正确的是
A.工业上制取粗硅的化学方程式:SiO2+2C Si+2CO↑
Si+2CO↑
B.硫酸型酸雨的形成会涉及反应2H2SO3 +O2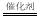 2H2SO4
2H2SO4
C.Na2S2O3溶液中加入稀硫酸:S2O32-+2H+=SO2↑+S↓+H2O
D.已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量CO2:2ClO-+CO2+H2O=2HClO+CO32-
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨师大附中高三上学期期中考试化学试卷(解析版) 题型:选择题
六种短周期元素A、B、C、D、E、F的原子序数依次增大,其中A与E,B与F同主族,E与F同周期;D的核电荷数是F的最外层电子数的2倍;B的最高正价与最低负价的代数和为0;常温下单质A与E的状态不同。下列判断正确的是
A.A、C两种元素只能组成化学式为CA3的化合物
B.F与D形成的化合物性质很不活泼,不与任何酸反应
C.原子半径由大到小的顺序是E>F>C>D
D.元素的非金属性由强到弱的顺序是D>C>F>B
查看答案和解析>>
科目:高中化学 来源:2016届河南省高三上学期第八次大考化学试卷(解析版) 题型:选择题
光谱研究表明,易溶于水的SO2所形成的溶液中存在着下列平衡:

据此,下列判断中正确的是
A.该溶液中存在着SO2分子
B.该溶液中H+浓度是SO32-浓度的2倍
C.向该溶液中加入足量的酸SO2气体都能放出
D.向该溶液中加入NaOH可得到Na2SO3、NaHSO3和NaOH的混合溶液
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
向27.2Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO 和Cu(NO3)2。在所得溶液中加入1.0mol/L 的NaOH溶液1.0L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g。下列说法正确的是( )
A.Cu与Cu2O 的物质的量之比为1:2
B.产生的NO的体积为4.48L
C.硝酸的物质的量浓度为2.6mol/L
D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林实验中学高二上学期期中考试化学试卷(解析版) 题型:选择题
有两种一元弱酸的钠盐溶液,其物质的量浓度相等,现向这两种盐的溶液中分别通入适量的CO2,发生如下反应:NaR+CO2+H2O=HR+NaHCO3 2NaR1+CO2+H2O=2HR1+Na2CO3。HR和HR1的酸性强弱比较,正确的是( )
A.HR较B弱 B.HR1较弱 C.两者相同 D.无法比较
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高级中学高三上学期期中考试化学试卷(解析版) 题型:填空题
蓄电池是一种反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应如下:NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
(1)此蓄电池在充电时,电池负极应与外加电源的_____极连接,电极反应式为_____________。
(2)以铜为电极,用此蓄电池作电源,电解以下溶液,开始阶段发生反应:
Cu+2H2O===Cu(OH)2+H2↑的有__________ ____。
____。
A.稀H2SO4 B.NaOH溶液 C.Na2SO4溶液 D.CuSO4溶液 E.NaCl溶液
(3)假如用此蓄电池电解以下溶液 (电解池两极均为惰性电极),工作一段时间后,蓄电池内部消耗了0.36 g水。试回答下列问题:
(电解池两极均为惰性电极),工作一段时间后,蓄电池内部消耗了0.36 g水。试回答下列问题:
①电解足量N(NO3)x溶液时某一电极析出了a g金属N,则金属N的相对原子质量R的计算公式为R=____________(用含a、x的代数式表示)。
②电解含有0.1 mol·L-1的CuSO4溶液100 mL,阳极产生标准状况下的气体体积为________L;将电解后的溶液加水稀释至2L,溶液的pH=_____。
(4)熔融盐燃料电池是以熔融碳酸盐为电解质、CH4为燃料、空气为氧化剂、稀土金属材料为电极的新型电池。已知该熔融盐电池的负极的电极反应是:CH4-8e-+4 CO=5CO2+2H2O,则正极的电极反应式为_______________________。
(5)有一种用CO2生产甲醇燃料的方法:
已知:CO2(g)+3H2(g)===CH3OH(g)+H2O(g) ΔH=-a kJ·mol-1;
CH3OH(g)===CH3OH(l) ΔH=-b kJ·mol-1;
2H2(g)+O2(g)===2H2O(g) ΔH=-c kJ·mol-1;
H2O(g)===H2O(l) ΔH=-d kJ·mol-1。
则表示CH3OH(l)燃烧热的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016届贵州省遵义市高三上学期第一次联考化学试卷(解析版) 题型:选择题
金属在人类社会的发展进程中起着重要的作用。下列有关金属及其化合物的说法正确的是
A.Fe、Mg、Al均能与空气中的氧气反应在表面生成致密的氧化膜,对内层金属有保护作用
B.Fe在高温下能与水蒸气反应,Fe被氧化生成Fe2O3,H2O被还原生成H2
C.鉴别Na2CO3和NaHCO3溶液可向两种溶液中加入Ba(OH)2溶液,产生沉淀的就是Na2CO3
D.Al与NaOH溶液的反应中,NaOH既不是氧化剂又不是还原剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com