
����Ŀ����A��B��C��D��E����Ԫ�أ����ǵĺ˵�������������Ҷ�С��20������AΪ�ǽ���Ԫ�أ�A��E����ͬһ�壬����ԭ�ӵ����������Ų�ʽΪns1��B��DҲ����ͬһ�壬����ԭ��������p�ܼ���������s�ܼ���������������Cԭ��������ϵ���������Dԭ��������ϵ�������һ�롣��ش��������⣺
��1��A��____��B��____��C��_____��D��____��E��____��
��2����������Ԫ����ɵ�һ�ֻ�������(д��ѧʽ)____��д�������ʵ�һ����Ҫ��;��____��
��3��д��CԪ�ػ�̬ԭ�ӵĵ����Ų�ʽ��___��
��4���õ����Ų�ͼ��ʾDԪ��ԭ�ӵ���Χ�����Ų�Ϊ____��
���𰸡�H O Al S K KAl(SO4)2��12H2O ��ˮ�� 1s22s22p63s23p1 ![]()
��������
A��E��ͬ��,����ԭ�ӵ����������Ų�ʽΪns1��˵��A��Eλ�ڵ�IA�壬��A���ǽ�������AΪH��B��DҲ��ͬ��,����ԭ��������p�ܼ���������s�ܼ�����������������B��DΪ��VIA��Ԫ�أ���ôBΪO��DΪS��Cԭ�ӵ���������������Dԭ�ӵ�������������һ�룬��ôCΪAl������Ԫ�غ˵������������֪EΪK���ɴ˷�����
��1���ɷ�����֪AΪH��BΪO��CΪAl��DΪS��EΪK��
��2������������Ԫ����ɵ�����ΪKAl(SO4)2��12H2O���dz����ľ�ˮ����
��3��CΪAl����̬ԭ�ӵĵ����Ų�ʽΪ1s22s22p63s23p1��
��4��DΪS�������Ų�ʽΪ1s22s22p63s23p4����Χ�����Ų�ʽΪ3s23p4����Χ�����Ų�ͼΪ![]() ��
��


 ���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д�
���Ͱ�ͨ�������Сѧ��ʱͬ�����ϵ�д� ���Ͱ�ͨ������ϵ�д�
���Ͱ�ͨ������ϵ�д� �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����д�С�Ƚ���ȷ����
A. ������������ʵ���Ũ�ȵ�NaCl(aq)��������С��NaClO(aq)����������
B. 25 ��ʱ��pH��3��������Һ��ˮ�ĵ���̶ȴ���pH��11�İ�ˮ��ˮ�ĵ���̶�
C. 0.1 mol��L��1(NH4)2CO3��Һ�е�c(NH![]() )����0.1 mol��L��1��NH4Cl��Һ�е�c(NH
)����0.1 mol��L��1��NH4Cl��Һ�е�c(NH![]() )��2��
)��2��
D. �����£��������ơ���������Һ��Ϻ���Һ�����ԣ���Һ��c(Na��)����c(Cl��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£�0.1 mol��L1 H2R��Һ��H2R��HR��R2��������ռ���ʵ����������ֲ�ϵ���ģ���pH�仯�Ĺ�ϵ��ͼ��ʾ�����б�����ȷ����
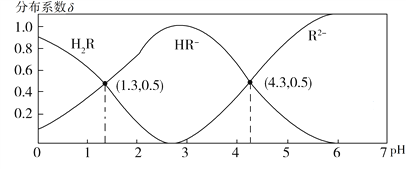
A. Na2R��Һ�У�c(Na+)=c(HR)+2c(R2)
B. H2R![]() H++HR��Ka1=1.0��101.3
H++HR��Ka1=1.0��101.3
C. �����ʵ�����NaHR��Na2R����ˮ��ʹ����ҺpHǡ��Ϊ4.3
D. HF��Ka=1.0��103.4��������NaF��Һ�м�������H2R��������Ӧ��H2R+2F![]() 2HF+R2
2HF+R2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ������������������β������Ⱦ����ŷ�������������Ҫ��װ��Ԫ������
(1)��Ԫ���������ô���������β���е�������Ҫ��Ⱦ��ת��Ϊ�����ʡ���������Ҫ��Ⱦ���ǣ�![]() ��_____��________��д���ڴ��������£�������ԭ
��_____��________��д���ڴ��������£�������ԭ![]() �Ļ�ѧ����ʽ��_________���ڸ÷�Ӧ����������ͻ�ԭ��������ʵ���֮��Ϊ______��
�Ļ�ѧ����ʽ��_________���ڸ÷�Ӧ����������ͻ�ԭ��������ʵ���֮��Ϊ______��
(2)���������ü״����Һ��ʯ������Ϊ��������ȼ�ϣ��״���Ϊ������ȼ�ϵĺô���_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1molI2��g����2molH2����5L�ܱ������У���һ���¶��·�����Ӧ��I2��g����H2��g��![]() 2HI��g����H<0�����ﵽƽ�⡣HI���������w��HI����ʱ��仯�����ߣ�������ʾ��
2HI��g����H<0�����ﵽƽ�⡣HI���������w��HI����ʱ��仯�����ߣ�������ʾ��
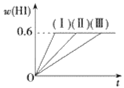
��1���ﵽƽ��ʱ��I2��g�������ʵ���Ũ��Ϊ________��
��2�����ı䷴Ӧ�������ڼ�������w��HI���ı仯�����ߣ�������ʾ������������w��HI���ı仯�����ߣ�������ʾ���������������________��������������________������������������ţ���
�����������£������¶�
�����������£������¶�
�����������£���С��Ӧ�������
�����������£�����Ӧ�������
�����º��������£������ʵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 ��ʱ��x mol��L��1�����ˮ��Һ�У�����KOH���������Һ��pH(���Լ�������������Һ����仯)���õ�c(HF)��c(F��)����ҺpH�ı仯��ϵ��ͼ��ʾ������˵����ȷ���� (����)��

A.��c(F��)>c(HF)ʱ����Һ�ʼ���
B.��pH��2ʱ��c(F��)<c(K��)
C.25 ��ʱ�������ĵ���ƽ�ⳣ��Ϊ4��10��6
D.��pH��5ʱ��c(HF)��c(K��)��c(H��)��c(OH��)��x mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����Һ��˵������ȷ����
A.��![]() Ϊ�����ӵ�������500mL
Ϊ�����ӵ�������500mL![]() �Ȼ�����Һ��
�Ȼ�����Һ��![]() ����ĿС��
����ĿС��![]()
B.�����£���![]() ��HCOONa��Һ�У�
��HCOONa��Һ�У�![]()
C.��ͬ���ʵ���Ũ�ȵ�������Һ��![]()
![]() ��
��![]() �ɴ�С��˳���ǣ�
�ɴ�С��˳���ǣ�![]()
D.��Ȼ��ر���ԭ��ͭ���������������ú��Ϊ![]() ��Һ����������ZnS��ת��ΪCuS��˵��CuS���ܽ��С��ZnS
��Һ����������ZnS��ת��ΪCuS��˵��CuS���ܽ��С��ZnS
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ����25mL 0.1mol��L-1������������Һ�У���μ���0.2mol��L-1 CH3COOH��Һ����Һ��pH�仯������ͼ��ʾ�����з���������ȷ���ǣ� ��
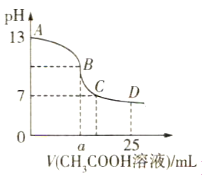
A.��B������a=12.5������c(Na+)=c(CH3COO-)
B.��������A��B������һ�㣬��Һ�ж���c(Na+)��c(OH-)��c(CH3COO-)��c(H+)
C.D��ʱ��c(CH3COO-)+c(CH3COOH)=c(Na+)
D.C��ʱ��c(CH3COO-)=c(Na+)��c(H+)=c(OH-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��11.2L���顢���顢��ȩ��ɵĻ�����壬��ȫȼ�պ�����15.68L CO2(����������ڱ�״���²ⶨ)��������������������ٷֺ���Ϊ�� ��
A.80��B.60��C.40��D.20��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com