
【题目】将1molI2(g)和2molH2置于5L密闭容器中,在一定温度下发生反应:I2(g)+H2(g)![]() 2HI(g)ΔH<0,并达到平衡。HI的体积分数w(HI)随时间变化如曲线(Ⅱ)所示:
2HI(g)ΔH<0,并达到平衡。HI的体积分数w(HI)随时间变化如曲线(Ⅱ)所示:
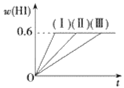
(1)达到平衡时,I2(g)的物质的量浓度为________。
(2)若改变反应条件,在甲条件下w(HI)的变化如曲线(Ⅰ)所示,在乙条件下w(HI)的变化如曲线(Ⅲ)所示。则甲条件可能是________,乙条件可能是________(填入下列条件的序号)。
①恒容条件下,升高温度
②恒容条件下,降低温度
③恒温条件下,缩小反应容器体积
④恒温条件下,扩大反应容器体积
⑤恒温恒容条件下,加入适当催化剂
【答案】0.02mol/L ③⑤ ④
【解析】
(1)混合气体总的物质的量不变,根据平衡时HI的体积分数计算![]() ,根据方程式知道转化的碘的物质的量,进而计算平衡时碘的物质的量,再根据
,根据方程式知道转化的碘的物质的量,进而计算平衡时碘的物质的量,再根据![]() 计算;
计算;
(2)由图可知,改变条件平衡不移动,甲的速率增大、乙的速率降低,据此结合外界条件对反应速率与平衡移动的影响判断。
混合气体总的物质的量不变,平衡时,![]() 由方程式可以知道,转化的碘的物质的量=
由方程式可以知道,转化的碘的物质的量=![]() ,平衡时碘的物质的量=1mol-0.9mol=0.1mol,平衡时,I2(g)的物质的量浓度为
,平衡时碘的物质的量=1mol-0.9mol=0.1mol,平衡时,I2(g)的物质的量浓度为![]() ,故答案为:0.02mol/L。
,故答案为:0.02mol/L。
(2)由图可以知道,改变条件平衡不移动,甲的速率增大、乙的速率降低,
①恒容条件下,升高温度,平衡向逆反应移动,
②恒容条件下,降低温度,平衡向正反应方向移动,
③恒温条件下,缩小反应容器体积,压强增大,平衡不移动,反应速率增大,
④恒温条件下,扩大反应容器体积,压强减小,平衡不移动,反应速率减小,
⑤恒温恒容条件下,加入适当催化剂,平衡不移动,反应速率增大,
故甲条件可能是③⑤,乙条件可能是④,故答案为:③⑤;④。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.c(OH-)=1×10-13mol/L的溶液中:Mg2+、K+、SO42-、NO3-
B.![]() =1×10-10的溶液中:Na+、Cu2+、HCO3-、NO3-
=1×10-10的溶液中:Na+、Cu2+、HCO3-、NO3-
C.0. 1 mol·L-1KNO3 溶液:H+、K+、SO42-、I-
D.0. 1 mol·L-1NaHS 溶液: H+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)===PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是
A. 反应在前50 s的平均速率v(PCl3)=0.0032 mol·L-1·s-1
B. 保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L-1,则反应的ΔH<0
C. 相同温度下,起始时向容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,反应达到平衡前v(正)>v(逆)
D. 相同温度下,起始时向容器中充入2.0 mol PCl3和2.0 mol Cl2,达到平衡时,PCl3的转化率小于80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含手性碳原子的分子称手性分子,手性分子具有光学活性。如下图有机物具有光学活性(式中标有*号的为手性碳原子),也能发生下列反应,请问发生哪种反应后,该有机物仍然一定具有光学活性( )
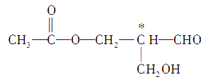
A. 消去反应 B. 水解反应 C. 银镜反应 D. 酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】安全气囊是行车安全的重要设施,当车辆发生碰撞的瞬间,安全装置通电点火使其中的粉末分解释放出大量的氮气形成气囊,从而保护司机及乘客的安全。为研究安全气囊工作的化学原理,取安全装置中的粉末进行研究。经实验分析,确定该粉末是一种混合物且只含Na、Fe、N、O四种元素。
(1)氧元素在元素周期表中的位置是__________,Na原子的结构示意图为__________,Na、Fe、N、O四种元素中三种主族元素的离子半径从大到小的顺序是__________(用离子符号表示)。
(2)水溶性实验表明,安全装置中固体粉末部分溶解。不溶物为一种红棕色固体,可溶于盐酸。已知该不溶物能发生铝热反应,写出该反应的化学方程式:___________。
(3)氮的最高价氧化物对应的水化物与其氢化物反应生成一种盐,该盐中含有的化学键类型是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种元素,它们的核电荷数依次增大,且都小于20。其中A为非金属元素,A和E属于同一族,它们原子的最外层电子排布式为ns1。B和D也属于同一族,它们原子最外层的p能级电子数是s能级电子数的两倍,C原子最外层上电子数等于D原子最外层上电子数的一半。请回答下列问题:
(1)A是____,B是____,C是_____,D是____,E是____。
(2)由这五种元素组成的一种化合物是(写化学式)____。写出该物质的一种主要用途:____。
(3)写出C元素基态原子的电子排布式:___。
(4)用电子排布图表示D元素原子的外围电子排布为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,有A、B、C、D四种无色溶液,它们分别是![]() 溶液、
溶液、![]() 溶液、盐酸和
溶液、盐酸和![]() 溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。
溶液中的一种。已知A、B的水溶液中水的电离程度相同,A、C溶液的pH相同。
则:①B是________溶液,C是________。
②常温下若B溶液中![]() 与C溶液中
与C溶液中![]() 相同,B溶液的pH用
相同,B溶液的pH用![]() 表示,C溶液的pH用
表示,C溶液的pH用![]() 表示,则
表示,则![]() ________(填某个数)。
________(填某个数)。
(2)已知某溶液中只存在![]() 四种离子,某同学推测其离子浓度大小顺序可以有以下几种可能:
四种离子,某同学推测其离子浓度大小顺序可以有以下几种可能:
①![]()
②![]()
③![]()
④![]()
则:
(i)上述关系一定不正确的是________(填序号)。
(ii)若溶液中只有一种溶质,则该溶液中离子浓度的大小关系为________(填序号)。
(iii)若四种离子浓度关系有![]() ,则该溶液显________(填“酸性”“碱性”或“中性”)。
,则该溶液显________(填“酸性”“碱性”或“中性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2mol/L一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是

A. HA是强酸
B. 该混合液pH=7
C. 图中x表示HA,Y表示OH-,Z表示H+
D. 该混合溶液中:c(A-)+c(Y)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知293K时下列物质的溶度积![]() 单位已省略
单位已省略![]() :
:
| Ag2SO4 | FeS | CuS | Ag2S |
| 1.2×10-5 | 6.3×10-18 | 8.5×10-45 | 6.3×10-50 |
下列说法正确的是![]()
![]()
A.相同温度下,Ag2SO4、FeS、CuS饱和溶液中:![]()
B.向FeS悬浊液中滴加CuSO4溶液发生反应的离子方程式:![]()
C.浓度均为0.004mol/L的AgNO3和H2SO4溶液等体积混合后不能产生沉淀
D.向饱和Ag2S溶液中加少量Na2S固体,溶液中c(Ag+)不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com