
 可逆反应aA(g)+bB(g)?cC(g)+dD(g)的v-t图象如图所示.
可逆反应aA(g)+bB(g)?cC(g)+dD(g)的v-t图象如图所示.分析 ①反应开始到平衡时,根据△c=vt确定阴影部分含义;
②催化剂只影响化学反应速率但不影响平衡移动.
解答 解:①反应开始到平衡时,根据△c=vt知,阴影部分为速率与时间乘积,所以为反应物A的浓度减少量,
故答案为:反应物A的浓度减少量;
②催化剂能降低反应所需活化能,增大活化分子百分数,从而增大活化分子之间的有效碰撞,能同等程度的增大正逆反应速率,但不改变平衡移动,所以反应达到平衡状态时反应物的物质的量改变量不变,则阴影部分面积不变,
故答案为:不变.
点评 本题考查v-t图象分析,明确纵横坐标及阴影部分含义是解本题关键,知道外界条件对化学反应速率及化学平衡的影响原理,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 增大 | B. | 减小 | C. | 不变 | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a(A)>a′(A) a(B)<a′(B) | B. | a(A)>a′(A) a(B)=a′(B) | C. | a(A)<a′(A) a(B)<a′(B) | D. | a(A)=a′(A) a(B)>a′(B) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是用于合成药物的中间体.请根据下列转化关系图回答有关问题:
)是用于合成药物的中间体.请根据下列转化关系图回答有关问题:
 .
. .
. )是对甲基苯甲酸乙酯的同分异构体,下列物质与其能发生反应的是ACD(填序号).
)是对甲基苯甲酸乙酯的同分异构体,下列物质与其能发生反应的是ACD(填序号). +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$ +H2O.
+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单位时间内生成n mol的AB的同时,生成n mol的A2 | |
| B. | 单位时间内生成n mol A2的同时,生成n mol的B2 | |
| C. | 容器内的总压强不随时间而变化 | |
| D. | 单位时间内生成2n mol AB的同时,生成n mol的B2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
. ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
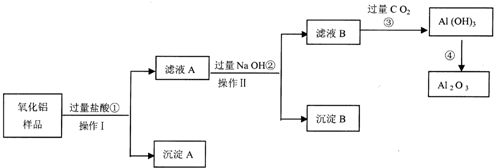
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:HClO4>H2SO4>H3PO4 | B. | 热稳定性:H2S>H2O>HF | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 氧化性:F2>Cl2>Br2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com