
1.52g 铜镁合金完全溶解于50mL 密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况),向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是( )
A.该合金中铜与镁的物质的量之比是2:1
B. 该浓硝酸中HNO3的物质的量浓度是14.0 mol/L
C.NO2和N2O4的混合气体中,NO2的体积分数是80%
D.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mLzxxk
科目:高中化学 来源: 题型:
有以下6种物质,结合相关问题填空:
①Al ②FeCl3溶液 ③SO2 ④碱石灰 ⑤氨气 ⑥NaOH固体
(1)能导电的是(填序号,以下同) ;属于非电解质的是 ;
常用作干燥剂的是 。
(2)①与⑥溶液反应的化学方程式为: 。
(3)向②溶液中加入KI溶液后,用CCl4萃取,CCl4层呈紫色,写出该反应过程的离子方程式: 。
(4)某化学实验小组同学利用以下装置制备⑤,并探究⑤的性质(部分仪器已略去)。

i.实验室制备⑤的化学方程式为 。
ii.收集⑤时,请你选择进气口 (填“a”或“b”)。
iii.着观察到装置B中的烧瓶内产生了红色喷泉,则说明⑤具有的性质是 。
iv.将产生的氨气缓慢通入②溶液中,观察到的现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组的同学在分析甲酸的组成和结构后,对甲酸的性质提出如下猜想并设计了相关实验加以验证:
猜想Ⅰ:甲酸具有酸性
实验Ⅰ:在甲酸溶液中滴加紫色石蕊试液
猜想Ⅱ:甲酸能发生酯化反应
实验Ⅱ:[装置如图(1)所示]
猜想Ⅲ:甲酸能发生银镜反应
实验Ⅲ:[步骤如图(2)所示]
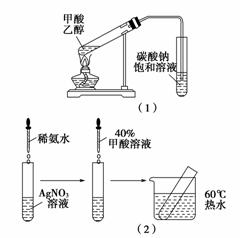
问题Ⅰ:请你进一步设计实验证明甲酸是强酸还是弱酸:______________________________________________。
问题Ⅱ:实验Ⅱ能验证猜想Ⅱ吗?________;如能,请说明你的理由;如不能,请指出实验Ⅱ中的错误__________________________________________________。
问题Ⅲ:分析甲酸的结构,实验Ⅲ中没有出现任何现象的可能原因是_______________________________。
问题Ⅳ:请你在仔细分析甲酸的组成和结构的基础上,再提出一个关于甲酸性质的猜想并设计实验方案验证你的猜想:
(1)你提出的猜想是______________________。
(2)你设计的实验方案是__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
月球含有H、He、N、Na、Mg、Si等元素,是人类未来的资源宝库。
(1)3He是高效核能原料,其原子核内中子数为________。
(2)Na的原子结构示意图为________,Na在氧气中完全燃烧所得产物的电子式为________。
(3)MgCl在工业上应用广泛,可由MgO制备。
①MgO的熔点比BaO的熔点________(填“高”或“低”)。
②月球上某矿石经处理得到的MgO中含有少量SiO2,除去SiO2的离子方程式为__________________________;SiO2的晶体类型为________。
③MgO与炭粉和氯气在一定条件下反应可制备MgCl2。若尾气可用足量NaOH溶液完全吸收,则生成的盐为________________(写化学式)。
(4)月壤中含有丰富的3He,从月壤中提炼1 kg 3He,同时可得6000 kg H2和700 kg N2,若以所得H2和N2为原料经一系列反应最多可生产碳酸氢铵________kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质性质与应用对应关系正确的是( )
A.晶体硅熔点高硬度大,可用于制作半导体材料
B.氢氧化铝具有弱碱性,可用于制胃酸中和剂
C.漂白粉在空气中不稳定,可用于漂白纸张
D.氧化铁能与酸反应,可用于制作红色涂料
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的CuS和Cu2S的混合物投入足量的HNO3中,收集到气体VL(标准状况),向反应后的溶液中(存在Cu2+和SO42-)加入足量NaOH,产生蓝色沉淀,过滤,洗涤,灼烧,得到CuO12.0g,若上述气体为NO和NO2的混合物,且体积比为1﹕1,则V可能为
A.9.0L B.13.5 L C.15.7L D.16.8L
L C.15.7L D.16.8L
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可用铜和浓硫酸加热或硫酸和亚硫酸钠反应制取二氧化硫。
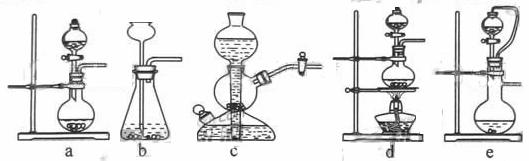
如果用硫酸和亚硫酸钠反应制取二氧化硫,并希望能控制反应速度,上图中可选用的发生装置是 (填写字母)。
41.若用硫酸和亚硫酸钠反应制取3.36L(标准状况)二氧化硫,至少需要称取亚硫酸钠
g(保留一位小数);如果已有4.0%亚硫酸钠(质量分数),被氧化成硫酸钠,则至少需称取该亚硫酸钠 g (保留一位小数)。
42.实验室二氧化硫尾气吸收与工业烟气脱硫的化学原理相通。石灰-石膏法和碱法是常用的烟气脱硫法。
石灰-石膏法的吸收反应为SO2+Ca(OH)2→CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O→2CaSO4·2H2O。其流程如下图:
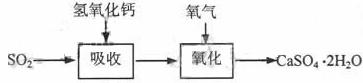
碱法的吸收反应为SO2+2NaOH→Na2SO3+H2O。碱法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如下图:
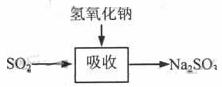
已知:
| 试剂 | Ca(OH)2 | NaOH |
| 价格(元/kg) | 0.36 | 2.90 |
| 吸收SO2的成本(元/mol) | 0.027 | 0.232 |
石灰-石膏法和碱法吸收二氧化硫的化学原理相同之处是 。和碱法相比,石灰-石膏法的优点是 ,缺点是 。
43.在石灰-石膏法和碱法的基础上,设计一个改进的、能实现物料循环的烟气脱硫方案(用流程图表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
由海水制备无水氯化镁,主要有以下步骤:①在一定条件下脱水干燥;②加熟石灰;③加盐酸;④过滤;⑤浓缩结晶。其先后顺序正确的是( )
A、②④⑤③①
B、③②④①⑤
C、③④②⑤①
D、②④③⑤①
查看答案和解析>>
科目:高中化学 来源: 题型:
将1.12克铁粉加入2摩/升氯化铁溶液25毫升中,充分的反应后,其结果是 ( )
A. 铁有剩余 B. 往溶液中滴入无色KSCN溶液,显红色
C. Fe2+与Fe3+物质的量之比为6 :1
D. 氧化产物与还原产物的物质的量之比为2 :5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com