解:(1)氯化铵和氢氧化钙发生复分解反应,生成氯化钙和氨气和水,故答案为:Ca(OH)
2+2NH
4Cl

CaCl
2+2H
2O+2NH
3↑;
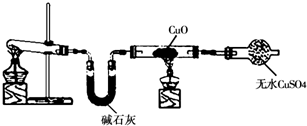
(2)①根据实验现象判断生成物,能使白色无水硫酸铜粉末变为蓝色的物质是水,黑色的氧化铜变为红色的物质是铜(类比氢气还原氧化铜),根据氧化还原反应得,该无色无污染的气体是氮气,故答案为:3CuO+2NH
3
3Cu+N
2+3H
2O;
②碱石灰的成分是 CaO和NaOH的混合物,CaO能和水反应,NaOH易潮解,所以能作干燥剂,
故答案为:吸收氨气中混有的水蒸气,防止干扰产物水的鉴定;
(3)①根据实验现象知,钠离子、硫酸根离子、硝酸根离子均不能单独使铜溶解,所以实验Ⅰ、Ⅱ、Ⅲ是证明铜和氢离子、钠离子、硫酸根离子和硝酸根离子都不反应,
故答案为:说明钠离子、硫酸根离子、硝酸根离子均不能单独使铜溶解;
②酸性条件下,铜和硝酸根离子发生氧化还原反应生成铜离子、一氧化氮气体和水,离子反应方程式为:3Cu+2NO
3-+8H
+=3Cu
2++2NO↑+4H
2O,故答案为:3Cu+2NO
3-+8H
+=3Cu
2++2NO↑+4H
2O;
③酸性条件下,向稀硫酸中加入铜后溶液变蓝色,说明铜被氧化生成铜离子,则双氧水被还原生成水,离子方程式为:Cu+2H
++H
2O
2=Cu
2++2H
2O,故答案为:Cu+2H
++H
2O
2=Cu
2++2H
2O.
分析:(1)实验室用氯化铵和氢氧化钙加热制取氨气;
(2)①先根据实验现象判断生成物,再根据元素守恒写出反应方程式;
②碱石灰是干燥剂;
(3)①实验Ⅰ、Ⅱ、Ⅲ是说明钠离子、硫酸根离子、硝酸根离子均不能单独使铜溶解;
②铜和稀硝酸反应生成一氧化氮和铜离子;
③酸性条件下,双氧水能把铜氧化成铜离子,自身被还原成水.
点评:本题考查了实验方案设计,明确物质的性质及其特殊性是解本题关键,利用对比实验结合实验现象得出结论,难度中等.

 CaCl2+2H2O+2NH3↑;
CaCl2+2H2O+2NH3↑; 3Cu+N2+3H2O;
3Cu+N2+3H2O; 

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案

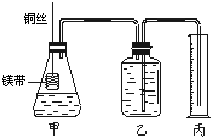 Ⅰ.铜与稀硝酸反应的离子方程式为
Ⅰ.铜与稀硝酸反应的离子方程式为