
(14分)Ⅰ(1)过渡金属元素有很多不同于主族元素的性质,如能形成多种配合物,如:Fe(CO)x、[Fe(H2NCONH2)6] (NO3)3 [三硝酸六尿素合铁(Ⅲ)]、[Cu(NH3)4]SO4等。
①Cu位于元素周期表第四周期第 族。
②配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于 (填晶体类型)。
(2)O和Na形成的一种只含有离子键的离子化合物的晶胞结构如图,距一个阴离子周围最近的所有阳离子为顶点构成的几何体为 。

Ⅱ(3)液化石油气中常存在少量有毒气体羰基硫(COS),必须将其脱除以减少环境污染和设备腐蚀。完成下列填空。
①写出羰基硫的电子式 ,羰基硫分子属于 (选填“极性”、“非极性”)分子。
②下列能说明碳与硫两元素非金属性相对强弱的是 。
A.相同条件下水溶液的pH:Na2CO3>Na2SO4 B.酸性:H2SO3>H2CO3
C.CS2中碳元素为+4价,硫元素为-2价
③羰基硫在水存在时会缓慢水解生成H2S,使溶液的pH约为6.5左右,此时钢铁设备会产生的电化学腐蚀主要是 。
Ⅰ(1)①ⅠB ;②分子晶体 ;(2)立方体
Ⅱ(3)①  ; 极性 ②A C ③吸氧腐蚀
; 极性 ②A C ③吸氧腐蚀
【解析】
试题分析:Ⅰ(1)①Cu是29号元素,核外电子排布是2、8、18、1,因此在元素周期表中位于第四周期第ⅠB。②配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于分子晶体。(2)由该离子化合物的晶胞结构示意图可知:与O2-最近的Na+构成是是立方体结构。Ⅱ(3)①羰基硫(COS)是CO2分子中的一个O原子被S原子代替的结构,所以羰基硫的电子式是 ;羰基硫分子属于极性分子;②A.NaOH是强碱,若某元素形成的含氧酸是强酸,则其水溶液是中性;若某元素形成的含氧酸是弱酸,则其钠盐呈碱性。因此相同条件下水溶液的pH:Na2CO3>Na2SO4可以证明C的非金属性比S弱。正确。B.元素的非金属性越强,该元素形成的最高价含氧酸的酸性越强,因此酸性:H2SO3>H2CO3.错误。C.两种非金属元素形成化合物,非金属性强的吸引电子能力就强,在化合物中显负化合价,元素非金属性弱的,在化合物中就表现正化合价。CS2中碳元素为+4价,硫元素为-2价,可以证明非金属性S>C。正确。③羰基硫在水存在时会缓慢水解生成H2S,发生反应的方程式是COS+H2O=H2S+CO2,使溶液的pH约为6.5左右,由于是弱酸性环境,所以此时钢铁设备会产生的电化学腐蚀主要是吸氧腐蚀。
;羰基硫分子属于极性分子;②A.NaOH是强碱,若某元素形成的含氧酸是强酸,则其水溶液是中性;若某元素形成的含氧酸是弱酸,则其钠盐呈碱性。因此相同条件下水溶液的pH:Na2CO3>Na2SO4可以证明C的非金属性比S弱。正确。B.元素的非金属性越强,该元素形成的最高价含氧酸的酸性越强,因此酸性:H2SO3>H2CO3.错误。C.两种非金属元素形成化合物,非金属性强的吸引电子能力就强,在化合物中显负化合价,元素非金属性弱的,在化合物中就表现正化合价。CS2中碳元素为+4价,硫元素为-2价,可以证明非金属性S>C。正确。③羰基硫在水存在时会缓慢水解生成H2S,发生反应的方程式是COS+H2O=H2S+CO2,使溶液的pH约为6.5左右,由于是弱酸性环境,所以此时钢铁设备会产生的电化学腐蚀主要是吸氧腐蚀。
考点:考查元素的推断、物质的分子结构、元素的非金属性强弱的比较的知识、金属腐蚀的类型的知识。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源:2013-2014重庆市下学期期中考试高二化学试卷(解析版) 题型:选择题
反应4A(g)+5B(g)== 4C(g)+ 6D(g)在某密闭容器中进行,半分钟后,C的物质的量浓度增加了0.3mol/L。下列论述正确的是( )
A.半分钟内的平均反应速率:5v(B)=6v(D) B.C的平均反应速率是0.010 mol·L-1·s-1
C.容器中含D的物质的量至少为0.45mol D.容器中A的物质的量浓度增加了0.3mol/L
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市高三5月月考理综化学试卷(解析版) 题型:选择题
(14分)有机物DBP常用作纤维素树脂和聚氯乙烯的增塑剂,特别适用于硝酸纤维素涂料。具有优良的溶解性、分散性和粘着性。由有机物A和邻二甲苯为原料可以合成DBP。
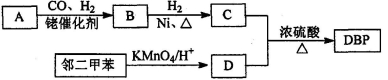
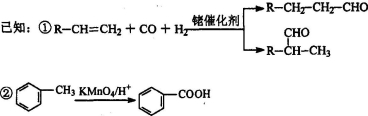
③烃A是有机合成的重要原料。A的质谱图表明其相对分子质量为42,红外光谱表明分子中含有碳碳双键;B能发生银镜反应;有机物C的核磁共振氢谱显示其分子中含有5种化学环境不同的氢原子,且个数之比为3:2:2:2:l。
回答下列问题:
(1)A的名称为___________;A在一定条件下生成聚合物的结构简式为___________________
(2)D中的含氧官能团是___________。有机物D和足量有机物C反应生成DBP的化学方程
式是____________________________________________
(3)下列说法正确的是___________ (选填序号字母)。
A.A能发生聚合反应、加成反应和氧化反应
B.与C互为同分异构体,且含有相同官能团的有机物有2种
C.邻二甲苯能氧化生成D说明有机物分子中基团之间存在影响
D.1 mol DBP可与含4mol NaOH的溶液完全反应
(4)工业上常用有机物E(C8H4O3)代替D生产DBP。反应分为两步进行:
i)E+C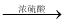 中间产物
中间产物
ii)中间产物+C  DBP+H2O
DBP+H2O
①请猜测E的结构简式___________。
②工业上生产有机物E的反应如下:2X+9O2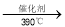 2E+4CO2+4H2O,芳香烃X的一溴代物只有两种。X的分子式是___________。
2E+4CO2+4H2O,芳香烃X的一溴代物只有两种。X的分子式是___________。
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市高三5月月考理综化学试卷(解析版) 题型:选择题
下列推论正确的是:
A.S(g)+O2(g)==SO2(g)△H1;S(s)+O2(g)==SO2(g) △H2,则:△H1>△H2
B.C(石墨,s)=C(金刚石,S)△H=+1.9 kJ/mol,则由石墨制取金刚石的反应是吸热反应,金刚石比石墨稳定
C.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(I)△H=﹣57.4 kJ/mol,则:含20 gNaOH的稀溶液与稀盐酸完全反应,放出的热量为28.7 kJ
D.2C(s)+O2(g)=2CO(g)△H=﹣221 kJ/mol,则碳的燃烧热等于110.5kJ/mol
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市六校高三5月第三次诊断性考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.在CuSO4溶液中加入PbS,可转变为铜蓝(CuS),则Ksp(PbS)<Ksp(CuS)
B.在NaHS溶液中,加入少量CuCl2粉末产生黑色沉淀,则pH增大
C.加热条件下并加入大量水促进TiCl4水解,以制备TiO2固体
D.铜制器皿放置过程中会生成铜绿是因为发生了析氢腐蚀
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市主城七区高三下学期第二次联考理综化学试卷(解析版) 题型:选择题
下列叙述中,不正确的是
A.pH=2与pH=1的CH3COOH溶液中,c(H+)之比为1 :10
B.1.0mol/ L的Na2CO3溶液中:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
C.仅含Na+、H+、OH-、CH3COO-离子的某溶液中可能存在:
c(Na+)>c(CH3COO-) >c(OH-)>c(H+)
D.0.1mol/ L的CH3COOH溶液中,由水电离出的c(H+)为1×10-13mol/ L
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆市下学期高三第二次诊断测试理科综合化学试卷(解析版) 题型:选择题
下列排列顺序不正确的是
A.熔点:Al>K>Na B.微粒的半径:Cl﹣>Na+>Mg2+>A13+
C.热稳定性:HF>HCl>HBr>HI D.仅结合质子能力:AlO2﹣>CO32﹣>F﹣
查看答案和解析>>
科目:高中化学 来源:2013-2014重庆一中高一下学期期末考试化学试卷(解析版) 题型:选择题
下列有关实验装置进行的相应实验,不能达到实验目的的是
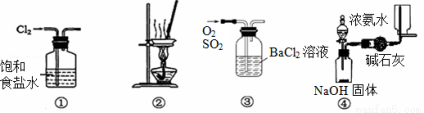
A.用装置①除去Cl2中含有的少量HCl
B.用装置②从KCl溶液中获得KCl晶体
C.用装置③除去O2中混有的一定量SO2
D.用装置④在实验室制取并收集氨气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com