
下列说法正确的是
A.沸点:H2O>H2S>H2Se>H2Te B.稳定性:SiH4>PH3>H2S >HCl
C.熔点:SiC >KCl> I2>CO2 D.沸点:CH4 >SiH4>GeH4>SnH4
C
【解析】
试题分析:A.这些都是同族元素形成的氢化物,结构相似。对于结构相似的物质,一般情况下,相对分子质量越大,分子间作用力就越大,物质的熔沸点就越高,但是由于在水的分子之间存在氢键,增加了分子之间的相互作用。所以沸点变化规律是:H2O>H2Te>H2Se >H2S。错误。B.元素的非金属性越强,其对应的简单氢化物的稳定性就越强,由于非金属性:Cl>S>P>Si,稳定性:SiH4< PH3< H2S < HCl 。错误。C.一般情况下,各类晶体的熔沸点规律是:原子晶体>离子晶体>分子晶体。对于分子晶体来说相对分子质量越大,分子间作用力就越大,物质的熔沸点就越高。SiC属于原子晶体;KCl属于离子晶体;I2和CO2 属于分子晶体,因此熔点:SiC >KCl> I2>CO2 。正确。D.这些氢化物结构相似。相对分子质量越大,分子间作用力就越大。物质的沸点就越高。因此沸点:CH4 < SiH4< GeH4< SnH4。错误。
考点:考查物质的熔沸点及稳定性的变化规律的知识。


 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:填空题
(3分)科学家一直致力于“人工固氮” 的方法研究。目前合成氨的技术原理为氮气和氢气在高温高压催化剂条件下生成氨气,一定条件下,向一个1L的密闭容器中充入2molN2和6molH2,反应达平衡时生成NH3的浓度为1 mol·L-1,并放出Q kJ热量,该反应的热化学方程式可表示为 ____ __。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高一下学期期末考试化学试卷(解析版) 题型:选择题
四种主族元素的离子a Xm+,bYn+,cZn-和dRm-(a,b,c,d为元素的原子序数),它们具有相同的电子层结构,若m>n,对下列叙述的判断正确的是( )
①a-b=n-m ②元素的原子序数a>b>c>d
③元素非金属性Z>R ④最高价氧化物对应水化物碱性X>Y
A.②③正确 B.只有③正确 C.①②③④正确 D.①②③正确
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高二化学试卷(解析版) 题型:填空题
(7分)决定物质性质的重要因素是物质结构。请回答下列问题:
(1)铜是过渡元素。化合物中,铜常呈现+1价或+2价。右图为某铜氧化物晶体结构单元,该氧化物的化学式为 。
(2)第三周期部分元素氟化物的熔点见下表:
氟化物 | NaF | MgF2 | SiF4 |
熔点/K | 1266 | 1534 | 183 |
解释MgF2与SiF4熔点差异的原因 。
(3)A和B为第三周期元素,其原子的部分电离能如下表所示:
电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
A | 578 | 1817 | 2745 | 11578 |
B | 738 | 1451 | 7733 | 10540 |
则A的电负性 B的电负性(填“>”、“<”或“=”)。
(4)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5、CrO2、Fe3O4中,更适合作录音带磁粉原料的是__________(填化学式)。
(5)实验室检验Ni2+可用丁二酮肟与之作用生成腥红色配合物沉淀。
②在配合物中用化学键和氢键标出未画出的作用力(镍的配位数为4)。
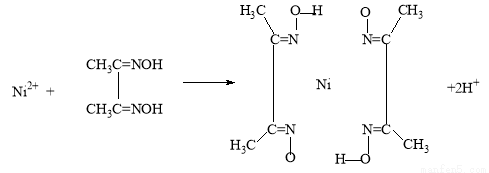
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高二化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中能大量共存的是( )
A.pH=1的溶液中:Na+、Fe2+、NO3-、SO42-
B.滴入酚酞试液显红色的溶液中:K+、Fe3+、ClO-、SO42-
C.c(H+)/c(OH-)=1×1012的溶液中:NH4-、Cl-、NO3-、Al3+
D.由水电离出的c(H+)=1×10-12mol/L的溶液中:Na+、K+、Cl-、HCO3-
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高二化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.前四周期中,原子最外层为1个电子的元素有5种
B.Fe2+的价电子排布为3d6
C.2p轨道上有1个未成对电子的原子与3p轨道上有1个未成对电子的原子化学性质相似
D.AB3型分子的中心原子A采取sp3杂化
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省“四地六校”下学期第三次联考高一化学试卷(解析版) 题型:填空题
根据元素周期表1~20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有____种,金属性最强的元素与氧气反应生成的化合物有______________(至少填两种化合物的化学式);
(2)属于稀有气体的是_________(填元素符号,下同);
(3)形成化合物种类最多的两种元素是__________________;
(4)第三周期中,原子半径最大的是(稀有气体除外)____________;
(5)推测Si、N最简单氢化物的稳定性由强到弱排列_____________(填化学式)。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建安溪一中、惠安一中、养正中学下学期期中高二化学(解析版) 题型:填空题
(14分) 氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
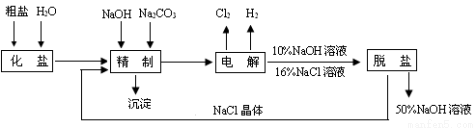
依据上图,完成下列填空:
在电解过程中,与电源正极相连的电极上所发生反应的方程式为: 。
与电源负极相连的电极附近溶液pH 。(填“不变”“增大”或“减小”)
(2)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该试剂可以选 。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)为有效除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为 (选a、b、c,多选扣分)。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(4)在用阳离子交换膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分反应,产物最终仅有NaClO和H2,相应的化学反应方程式为 、 。
查看答案和解析>>
科目:高中化学 来源:2013-2014甘肃省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列与化学概念有关的说法正确的是( )
A.化合反应均为氧化还原反应
B.催化剂能改变可逆反应达到平衡的时间
C.金属氧化物均为碱性氧化物
D.石油是混合物,其分馏产品汽油为纯净物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com