
【题目】设NA为阿伏加德罗常数,下列说法正确的是( )
A.32g O2气体含有的氧原子数为NA
B.2L 0.3mol/L Na2SO4溶液中含有Na+为0.6NA
C.27g铝完全反应后失去的电子数为3NA
D.11.2L氮气所含的分子数为0.5NA
 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:高中化学 来源: 题型:
【题目】在无色透明的溶液中,能大量共存的离子组是( )
A.K+、Cu2+、SO42-、Cl-
B.Na+、H+、Cl-、CO32-
C.H+、Ba2+、Cl-、NO3-
D.K+、Fe2+、OH-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子组合,能大量共存的是
A.酸性溶液中:Al3+、Fe3+、SO32-、Cl-
B.透明溶液中:MnO4-、K+、Na+、NO3-
C.强碱性溶液中:Na+、NO3-、SO32-、HCO3-
D.强酸性溶液中:Na+、Fe2+、SO42-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于乙烯(CH2=CH2)的说法不正确的( )
A. 乙烯分子中2个碳原子都是sp2杂化
B. 乙烯分子存在非极性键
C. 乙烯分子中4个H原子在同一平面上
D. 乙烯分子有6个σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种优质燃料,在工业上常用CO和H2合成甲醇,反应方程式为CO (g)+H2(g)![]() CH3OH(g)。已知:①CO(g)+1/2O2(g)=CO2(g) ΔH1=-283.0 kJ/mol;②H2(g)+1/2O2(g)=H2O(g) ΔH2=-241.8 kJ/mol;③CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH3=-192.2 kJ/mol。回答下列问题:
CH3OH(g)。已知:①CO(g)+1/2O2(g)=CO2(g) ΔH1=-283.0 kJ/mol;②H2(g)+1/2O2(g)=H2O(g) ΔH2=-241.8 kJ/mol;③CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH3=-192.2 kJ/mol。回答下列问题:
(1)计算CO(g)+2H2(g)![]() CH3OH(g)的反应热ΔH4=_________________。
CH3OH(g)的反应热ΔH4=_________________。
(2)若在绝热、恒容的密闭容器中充入1 mol CO、2 mol H2,发生反应CO(g)+2H2(g)![]() CH3OH(g),下列示意图正确且能说明在进行到t1时刻为平衡状态的是________(填选项字母)。
CH3OH(g),下列示意图正确且能说明在进行到t1时刻为平衡状态的是________(填选项字母)。

(3)T1℃时,在一个体积为5 L的恒容容器中充入1 mol CO、2 mol H2,经过5 min达到平衡,CO的转化率为0.8。T1℃时,在另一体积不变的密闭容器中也充入1 mol CO、2 mol H2,达到平衡时CO的转化率为0.7,则该容器的体积______5 L(填“>、<或=”);T1℃时,CO(g)+2H2(g)![]() CH3OH(g)的平衡常数K=____________。
CH3OH(g)的平衡常数K=____________。
(4)在T1℃时,在体积为5 L的恒容容器中充入一定量的H2和CO,反应达到平衡时CH3OH的体积分数与n(H2)/n(CO)的关系如图所示。温度不变,当n(H2)/n(CO)=2.5时,达到平衡状态,CH3OH的体积分数可能是图象中的________点。

(5)为了提高燃料的利用率可以将甲醇设计为燃料电池,写出KOH作电解质溶液时,甲醇燃料电池的负极反应式________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3是一种重要的化工原料,在生产、生活中用途广泛。
(1)已知:
共价键 | 键能/ kJ·mol-1 |
H―H | 436 |
N≡N | 946 |
N―H | 391 |
注:拆开气态物质中1 mol某种共价键需要吸收的能量,就是该共价键的键能。
N2 (g)+3 H2 (g)![]() 2 NH3 (g) H =____kJ·mol-1
2 NH3 (g) H =____kJ·mol-1
(2)一定温度下,向恒容的密闭容器中充入N2和H2发生反应:N2 +3H2 ![]() 2NH3,测得各组分浓度随时间变化如图1所示。
2NH3,测得各组分浓度随时间变化如图1所示。
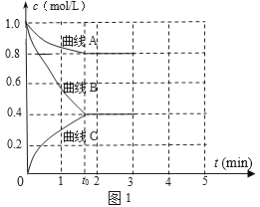
①表示c(N2)的曲线是__(填“曲线A”、“曲线B”或“曲线C”)。
②0~t0时用H2表示反应速率v(H2)____mol·L-1·min-1。
③下列能说明该反应达到平衡的是____。
a.混合气体的压强不再变化
b.2c(H2)= 3c(NH3)
c.混合气体的质量不再变化
d.NH3的体积分数不再变化
(3)潜艇中使用的液氨-液氧燃料电池工作原理如图2所示:
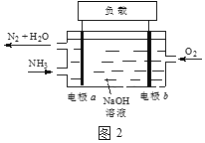
①电极b名称是____。
②电解质溶液中OH-离子向____移动(填“电极a”或“电极b”)。
③电极a的电极反应式为____。
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在乙烯分子中有5个σ键、一个π键,它们分别是( )
A.sp2杂化轨道形成σ键、未杂化的2p轨道形成π键
B.sp2杂化轨道形成π键、未杂化的2p轨道形成σ键
C.C﹣H之间是sp2形成的σ键,C﹣C之间是未参加杂化的2p轨道形成的π键
D.C﹣C之间是sp2形成的σ键,C﹣H之间是未参加杂化的2p轨道形成的π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲酸钠(![]() ,缩写为NaA)可用作饮料的防腐剂,研究表明苯甲酸(HA)的抑菌能力显著高于A-,已知25℃时,HA的Ka=6.25×10-5,H2CO3的Ka1=4.7×10-7,Ka2=4.90×10-11,在生产碳酸饮料的过程中除了添加NaA外,还需加压充入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)
,缩写为NaA)可用作饮料的防腐剂,研究表明苯甲酸(HA)的抑菌能力显著高于A-,已知25℃时,HA的Ka=6.25×10-5,H2CO3的Ka1=4.7×10-7,Ka2=4.90×10-11,在生产碳酸饮料的过程中除了添加NaA外,还需加压充入CO2气体,下列说法正确的是(温度为25℃,不考虑饮料中其他成分)
A. 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低
B. 提高CO2充气压力,饮料中c(A-)不变
C. 碳酸饮料中各种粒子的浓度关系为:c(H+)=c(HCO3-)+c(CO32-)+c(OH-)-c(HA)
D. 当pH为5.0时,饮料中![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com