
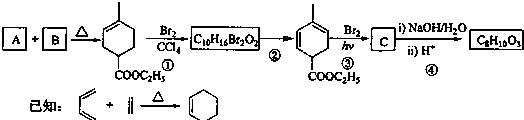
 ,根据异戊二烯和
,根据异戊二烯和 的结构简式知,A和B发生了加成反应,则B的结构简式为CH2=CHCOOCH2CH3,
的结构简式知,A和B发生了加成反应,则B的结构简式为CH2=CHCOOCH2CH3, 和溴发生加成反应生成
和溴发生加成反应生成 ,
, 在氢氧化钠的醇溶液、加热条件下发生消去反应生成
在氢氧化钠的醇溶液、加热条件下发生消去反应生成 .
. 和溴再光照条件下反应生成C,C和氢氧化钠的水溶液反应,再和酸反应生成C8H10O3,所以C的结构简式为:
和溴再光照条件下反应生成C,C和氢氧化钠的水溶液反应,再和酸反应生成C8H10O3,所以C的结构简式为: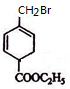 ,分子式为C8H10O3结构简式为
,分子式为C8H10O3结构简式为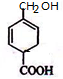 .
. ,根据异戊二烯和
,根据异戊二烯和 的结构简式知,A和B发生了加成反应,则B的结构简式为CH2=CHCOOCH2CH3,
的结构简式知,A和B发生了加成反应,则B的结构简式为CH2=CHCOOCH2CH3, 和溴发生加成反应生成
和溴发生加成反应生成 ,
, 在氢氧化钠的醇溶液、加热条件下发生消去反应生成
在氢氧化钠的醇溶液、加热条件下发生消去反应生成 .
. 和溴再光照条件下反应生成C,C和氢氧化钠的水溶液反应,再和酸反应生成C8H10O3,所以C的结构简式为:
和溴再光照条件下反应生成C,C和氢氧化钠的水溶液反应,再和酸反应生成C8H10O3,所以C的结构简式为: ,分子式为C8H10O3结构简式为
,分子式为C8H10O3结构简式为 ,
, +2NaOH
+2NaOH| 醇 |
| △ |
 +2NaBr+2H2O,
+2NaBr+2H2O, +2NaOH
+2NaOH| 醇 |
| △ |
 +2NaBr+2H2O;
+2NaBr+2H2O;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 前四周期的五种元素A、B、C、D、E原子序数逐渐变大,其中C、D元素同主族且原子序数D为C的二倍,B的第一电离能大于C,E原子的外围电子排布为(n-l)d (n+6)ns1.由它们组成的配位化合物X为深蓝色的结晶水合物,其原子个数比为14:4:5:1:1.回答下列问题.
前四周期的五种元素A、B、C、D、E原子序数逐渐变大,其中C、D元素同主族且原子序数D为C的二倍,B的第一电离能大于C,E原子的外围电子排布为(n-l)d (n+6)ns1.由它们组成的配位化合物X为深蓝色的结晶水合物,其原子个数比为14:4:5:1:1.回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:
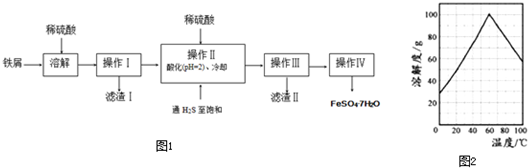
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 性质 |
| X | 其单质在潮湿的空气中放置表面易产生绿色的锈迹 |
| Y | 该元素在地壳中的含量仅次于氧 |
| Z | Z的氢化物能使湿润的红色石蕊试纸变蓝 |
| W | 单质为黄绿色气体,有毒 |
| T | T的一种核素质量数为32,其质子数与中子数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应过程中,分子的种类和数目一定发生改变 |
| B、如果某化学反应的△H和△S均小于0,则反应一定能自发进行 |
| C、化学反应过程中,一定有化学键的断裂和形成 |
| D、放热反应的反应速率,一定比吸热反应的反应速率快 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H+、Na+、NO3-、Cu2+ |
| B、Ba2+、Mg2+、Cl-、SO42- |
| C、Mg2+、K+、OH-、NO3- |
| D、NO3-、SO42-、K+、Mg2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com