
| ||
| A.只要反应时间充分就一定是4480mL |
| B.只要反应保持恒温就一定是4480mL |
| C.当满足反应时间充分和反应温度适当时可能是4480mL |
| D.即使满足反应时间充分和反应温度适当,也一定是少于4480mL |
科目:高中化学 来源:不详 题型:单选题
A.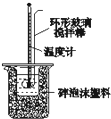 测定中和反应的反应热 |
B. 配制100mL 0.1mol/L盐酸 |
C.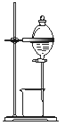 用来分离乙醇和水 |
D.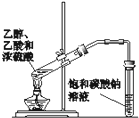 实验室制备乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
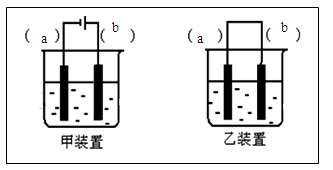
| A.一样多 | B.前者较后者多 |
| C.后者较前者多 | D.无法比较 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
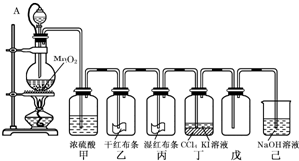
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
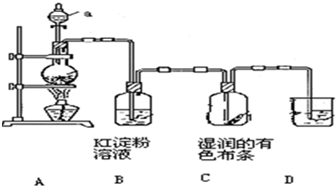
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
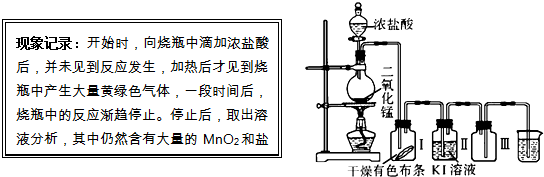
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
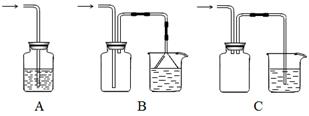
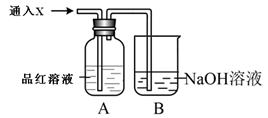
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com