
【题目】2015年10月中国药学家屠呦呦因发现青蒿素(一种用于治疗疟疾的药物)而获得诺贝尔生理医学奖.青蒿素(C15H22O5)的结构如图1所示.请回答下列问题:
(1)组成青蒿素的三种元素电负性由大到小排序是 , 在基态O原子中,核外存在对自旋相反的电子.
(2)下列关于青蒿素的说法正确的是(填序号).
a.青蒿素中既存在极性键又存在非极性键
b.在青蒿素分子中,所有碳原子均处于同一平面
c.图中数字标识的五个碳原子均只以σ键与其它原子成键
(3)在确定青蒿素结构的过程中,可采用NaBH4作为还原剂,其制备方法为:4NaH+B(OCH3)3→NaBH4+3CH3ONa
①NaH为离子晶体,如图2是NaH晶胞结构,则NaH晶体的配位数是 , 若晶胞棱长为a则Na原子间最小核间距为 .
②B(OCH3)3中B采用的杂化类型是 . 写出两个与B(OCH3)3具有相同空间构型的分子或离子 .
③NaBH4结构如图3所示.结构中存在的作用力有 .
【答案】
(1)O>C>H;3
(2)a
(3)6;![]() ;sp2;SO3、CO32﹣;离子键、配位键、共价键
;sp2;SO3、CO32﹣;离子键、配位键、共价键
【解析】(1)组成青蒿素的三种元素为H、C、O,元素的非金属性越强,电负性越强,非金属性:O>C>H,则H、C、O三种元素的电负性由大到小的顺序是O>C>H,;在基态O原子中,核外有8的电子,其中有3个轨道有成对电子,则核外存在3对自旋相反的电子,故答案为:O>C>H;3;(2)a.青蒿素中存在O﹣O键、C﹣C键,为非极性键,C﹣O、C﹣H键为极性键,故a正确;
b.含有饱和碳原子,具有烷烃的结构,则所有碳原子不处于同一平面,故b错误;
c.C=O键含有π键,故c错误;故答案为:a;(3)①NaH为离子晶体,NaH晶体中每个钠离子周围有6个氢负离子,若晶胞棱长为a,则Na原子间最小核间距为 ![]() ,故答案为:离子; 6;
,故答案为:离子; 6; ![]() ;②B(OCH3)3中B与3个O原子成键,为sp2杂化,B(OCH3)3的相同空间构型平面三角形,与B(OCH3)3具有相同空间构型的分子或离子可为SO3、CO32﹣ , 故答案为:sp2;SO3、CO32﹣;③B原子核最外层有3个电子,NaBH4存在离子键、配位键和共价键,故答案为:离子键、配位键、共价键.
;②B(OCH3)3中B与3个O原子成键,为sp2杂化,B(OCH3)3的相同空间构型平面三角形,与B(OCH3)3具有相同空间构型的分子或离子可为SO3、CO32﹣ , 故答案为:sp2;SO3、CO32﹣;③B原子核最外层有3个电子,NaBH4存在离子键、配位键和共价键,故答案为:离子键、配位键、共价键.
(1)组成青蒿素的三种元素为H、C、O,根据电负性的递变规律判断电负性的大小顺序;在基态O原子中,核外有8的电子,其中有3个轨道有成对电子;(2)a.青蒿素中存在O﹣O键、C﹣C键,为非极性键,C﹣O、C﹣H键为极性键;
b.含有饱和碳原子,具有烷烃的结构;
c.C=O键含有π键;(3)①NaH为离子晶体,NaH晶体中每个钠离子周围有6个氢负离子,若晶胞棱长为a,则Na原子间最小核间距为 ![]() ;②B(OCH3)3中B与3个O原子成键,B(OCH3)3的相同空间构型平面三角形;③NaBH4存在离子键、配位键和共价键.
;②B(OCH3)3中B与3个O原子成键,B(OCH3)3的相同空间构型平面三角形;③NaBH4存在离子键、配位键和共价键.


科目:高中化学 来源: 题型:
【题目】生物降解塑料袋由如图所示的塑料H制成,塑料H具有良好的生物相容性,可降解性能优良,机械性能及物理性能良好。塑料H既可以来源广泛且廉价的农副产品为原料合成,又可以甲烷为主要原料合成。以甲烷为主要原料合成塑料H的路线如下: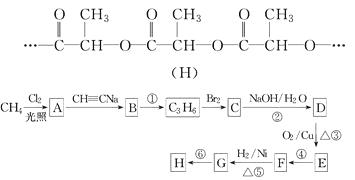
已知:CH3CH2X+CH3C≡CNa![]() CH3CH2C≡CCH3+NaX。
CH3CH2C≡CCH3+NaX。
请回答下列问题。
(1)反应①应控制的条件是 ,
反应④的类型是。
(2)写出下列反应的化学方程式:
反应②:
反应⑥:
(3)C的结构简式为 , 除C本身外,其同分异构体有种。
(4)根据你所学的知识,评价用甲烷合成塑料H的缺点: (写出两点即可)。
(5)根据塑料H的性能,指出其至少两种用途。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.抗酸药能中和胃里过多的盐酸,缓解胃部不适
B.碳酸镁、碳酸氢钠都能制成抗酸药
C.为防止过敏反应,患者使用青霉素前一定要进行皮肤敏感试验
D.中草药麻黄碱可用于治疗失眠、多梦等症状
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据最近的美国《农业研究》杂志报道,美国科学家发现半胱氨酸能增强艾滋病病毒感染者的免疫力,对控制艾滋病病毒的蔓延有奇效。已知半胱氨酸的结构简式为 ![]() ,则下列说法不正确的是( )
,则下列说法不正确的是( )
A.半胱氨酸属于α氨基酸
B.半胱氨酸是一种两性化合物
C.两分子半胱氨酸脱水形成的二肽的结构简式为
D. 与NaOH溶液加热时可放出一种碱性气体
与NaOH溶液加热时可放出一种碱性气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两种有机物的分子式相同,都可用CaHbOcNd表示,且a+c=b , a-c=d。已知A是天然蛋白质水解的最终产物;B是一种含有醛基的硝酸酯。试回答:
(1)A和B的分子式是。
(2)光谱测定显示,A的分子结构中不存在甲基,则A的结构简式为。
(3)光谱测定显示,B的烃基中没有支链,则B的结构简式为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2013年,“雾霾”成为年度关键词.近年来,对“雾霾”的防护与治理成为越来越重要的环境问题和社会问题.雾霾主要由二氧化硫、氮氧化物和可吸入颗粒物这三项组成.
(1)机动车的尾气是雾霾形成的原因之一,近几年有人提出利用选择性催化剂利用汽油中挥发出来的C3H6催化还原尾气中的NO气体,请写出该过程的化学方程式:
(2)我国北方到了冬季烧煤供暖所产生的废气也是雾霾的主要来源之一.经研究发现将煤炭在O2/CO2的气氛下燃烧,发现能够降低燃煤时NO的排放,主要反应为:
2NO(g)+2CO(g)N2(g)+2CO2(g)△H
若①N2(g)+O2(g)2NO(g)△H1=+180.5kJmol﹣1
②CO(g)C(s)+ ![]() O2(g)△H2=+110.5kJmol﹣1
O2(g)△H2=+110.5kJmol﹣1
③C (s)+O2(g)CO2(g)△H3=﹣393.5kJmol﹣1
则△H=kJmol﹣1 .
(3)燃煤尾气中的SO2用NaOH溶液吸收形成NaHSO3溶液,在pH为4~7之间时电解,硫元素在铅阴极上被电解还原为Na2S2O4 . Na2S2O4俗称保险粉,广泛应用于染料、印染、造纸、食品工业以及医学上.这种技术是最初的电化学脱硫技术之一.请写出该电解反应中阴极的电极方程式:
(4)SO2经过净化后与空气混合进行催化氧化后制取硫酸或者硫酸铵,其中SO2发生催化氧化的反应为:2SO2(g)+O2(g)2SO3(g).若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2(其中n(SO2):n(O2)=2:1),测得容器内总压强与反应时间如图所示:
①该反应的化学平衡常数表达式:K=
②图中A点时,SO2的转化率为
③计算SO2催化氧化反应在图中B点的压强平衡常数K=(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
④若在T2℃,其他条件不变的情况下测得压强的变化曲线如图所示,则T1T2(填“>”、“<”、“=”);其中C点的正反应速率vc(正)与A点的逆反应速率vA(逆)的大小关系为vc(正)vA逆) (填“>”、“<”、“=”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.青霉素有青霉素F、G、X、K、V等
B.青霉素G的俗名是盘尼西林
C.青霉素在体内水解可得到一类碱性物质
D.胃舒平、苏打片均属抗酸药
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁苯酞(J)是治疗轻、中度急性脑缺血的药物,合成J的一种路线如下:  已知:①
已知:① 
②E的棱磁共振氢谱只有一组峰;
③C能发生银镜反应;
④J是一种酯,分子中除苯环外还含有一个五元环.
回答下列问题:
(1)由A生成B的化学方程式为 ,其反应类型为 .
(2)D的化学名称是 ,由D生成E的化学方程式为 .
(3)J的结构简式为 .
(4)G的同分异构体中棱磁共振氢谱有4组峰且能与FeCl3溶液发生显色反应的结构筒式为(写出一种即可)
(5)由甲醛和化合物A经下列步骤可得到2一苯基乙醇. A ![]() K
K ![]() L
L ![]()
![]() CH2CH2OH反应条件1为 ;反应条件2所选择的试剂为;L的结构简式为 .
CH2CH2OH反应条件1为 ;反应条件2所选择的试剂为;L的结构简式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com