
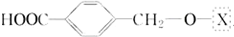
 ,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生.
,为了研究X的结构,将化合物A在一定条件下水解只得到B(分子式为C8H8O3)和C(分子式为C7H6O3).C遇FeCl3水溶液显紫色,与NaHCO3溶液反应有CO2产生. .
. (其中两种).
(其中两种). 为主要原料制备
为主要原料制备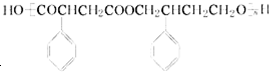 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下: .
. 分析 C遇FeCl3水溶液显紫色,与NaHCO2溶液反应有CO2产生,说明C中含有酚羟基和羧基,结合A的结构简式、B的分子式、C的分子式知,X前边的属于B中部分,所以B的结构简式为: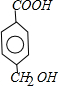 ,根据B的结构简式确定其具有的性质;C中含有羧基和酚羟基,根据RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH知,C中的羧基被含有生成醇羟基,所以D中含有酚羟基和醇羟基,D中醇羟基和氢溴酸发生取代反应生成E,E中含有酚羟基和溴原子,根据R-Br$→_{②H+}^{①NaCN}$R-COOH知,E中溴原子被取代生成羧基,在浓硫酸作催化剂、加热条件下,F发生酯化反应生成G,分子式为C8H6O2,分子内含有五元环,所以F发生分子内酯化反应生成G,则F的结构简式为:
,根据B的结构简式确定其具有的性质;C中含有羧基和酚羟基,根据RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH知,C中的羧基被含有生成醇羟基,所以D中含有酚羟基和醇羟基,D中醇羟基和氢溴酸发生取代反应生成E,E中含有酚羟基和溴原子,根据R-Br$→_{②H+}^{①NaCN}$R-COOH知,E中溴原子被取代生成羧基,在浓硫酸作催化剂、加热条件下,F发生酯化反应生成G,分子式为C8H6O2,分子内含有五元环,所以F发生分子内酯化反应生成G,则F的结构简式为: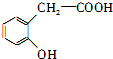 ,G的结构简式为:
,G的结构简式为: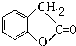 ,C的结构简式为:
,C的结构简式为: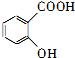 ,D的结构简式为:
,D的结构简式为: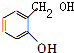 ,E的结构简式为:
,E的结构简式为: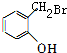 ,A的结构简式为:
,A的结构简式为: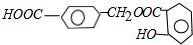 ,以
,以 为主要原料制备
为主要原料制备 ,可以用苯乙烯和溴发生加成反应生成
,可以用苯乙烯和溴发生加成反应生成 ,
,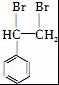 和氰化钠反应,然后酸化生成
和氰化钠反应,然后酸化生成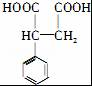 ,
,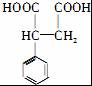 被还原生成
被还原生成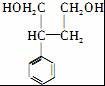 ,
,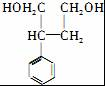 和
和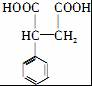 发生酯化反应生成
发生酯化反应生成 ,根据物质的结构和性质解答.
,根据物质的结构和性质解答.
解答 解:C遇FeCl3水溶液显紫色,与NaHCO2溶液反应有CO2产生,说明C中含有酚羟基和羧基,结合A的结构简式、B的分子式、C的分子式知,X前边的属于B中部分,所以B的结构简式为: ,根据B的结构简式确定其具有的性质;C中含有羧基和酚羟基,根据RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH知,C中的羧基被含有生成醇羟基,所以D中含有酚羟基和醇羟基,D中醇羟基和氢溴酸发生取代反应生成E,E中含有酚羟基和溴原子,根据R-Br$→_{②H+}^{①NaCN}$R-COOH知,E中溴原子被取代生成羧基,在浓硫酸作催化剂、加热条件下,F发生酯化反应生成G,分子式为C8H6O2,分子内含有五元环,所以F发生分子内酯化反应生成G,则F的结构简式为:
,根据B的结构简式确定其具有的性质;C中含有羧基和酚羟基,根据RCOOH$\stackrel{LiAlH_{4}}{→}$RCH2OH知,C中的羧基被含有生成醇羟基,所以D中含有酚羟基和醇羟基,D中醇羟基和氢溴酸发生取代反应生成E,E中含有酚羟基和溴原子,根据R-Br$→_{②H+}^{①NaCN}$R-COOH知,E中溴原子被取代生成羧基,在浓硫酸作催化剂、加热条件下,F发生酯化反应生成G,分子式为C8H6O2,分子内含有五元环,所以F发生分子内酯化反应生成G,则F的结构简式为: ,G的结构简式为:
,G的结构简式为: ,C的结构简式为:
,C的结构简式为: ,D的结构简式为:
,D的结构简式为: ,E的结构简式为:
,E的结构简式为: ,A的结构简式为:
,A的结构简式为: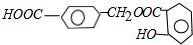 ,
,
(1)A的结构简式知,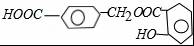 ,所以A中含有酯基、酚羟基和羧基,
,所以A中含有酯基、酚羟基和羧基,
故答案为:酯基;
(2)B的结构简式为: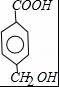 ,所以B能发生取代反应、加成反应和缩聚反应,故选abc;
,所以B能发生取代反应、加成反应和缩聚反应,故选abc;
(3)①C的结构简式为: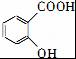 ,
,
故答案为: ;
;
②符合条件的E的同分异构体为: ,
,
故答案为: (其中两种);
(其中两种);
(4)苯乙烯和溴发生加成反应生成 ,
,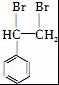 和氰化钠反应,然后酸化生成
和氰化钠反应,然后酸化生成 ,
, 被还原生成
被还原生成 ,
, 和
和 发生酯化反应生成
发生酯化反应生成 ,所以其合成路线为:
,所以其合成路线为: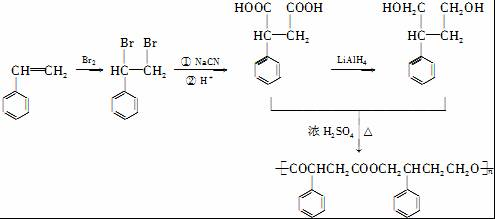 ,
,
故答案为: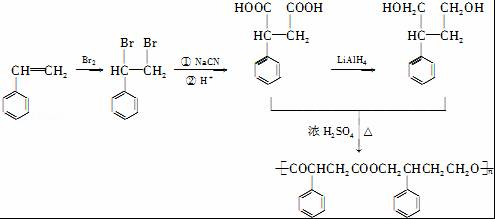 .
.
点评 本题考查有机物的推断及合成,明确有机物的官能团及性质是解本题关键,采用正、逆推相结合的方法进行分析,难点是设计合成路线,要求学生不仅掌握有机物的结构、性质还要掌握其反应条件,明确有机物的断键方式,难度较大.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:高中化学 来源: 题型:选择题
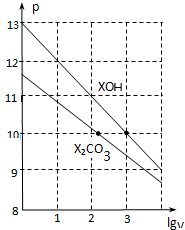
| A. | pH=10的两种溶液中的c(X+):XOH大于X2CO3 | |
| B. | 已知常温下,0.1 mol•L-1 XHCO3溶液的pH=8.31,则Ka1(H2CO3)•Ka2(H2CO3)>Kw | |
| C. | 已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2 | |
| D. | 当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则$\frac{c(HC{{O}_{3}}^{-})}{c(C{{O}_{3}}^{2-})}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
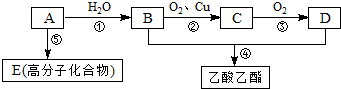
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 是一种抗氧化药物,存在如图所示的转化关系.
是一种抗氧化药物,存在如图所示的转化关系.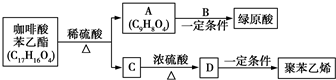
 .
.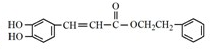 .
. (任写1个).
(任写1个).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
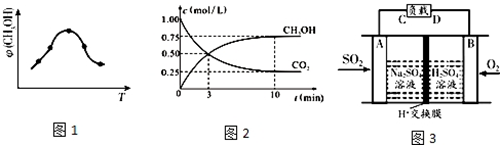
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3、NaHCO3两种盐的溶液中,离子种类不相同 | |
| B. | 常温下1mol/L的CH3COOH溶液与1mol/L的NaOH溶液等体积混合,所得混合液中c (CH3COO-)>c(Na+)>c(OH-)>c(H+) | |
| C. | 溶质的物质的量浓度相同的NH4Cl和NH4HSO4两种溶液中,c(NH4+)前者小于后者 | |
| D. | 常温下,某溶液中由水电离出的c(H+)为10-5mol/L,则此溶液可能是盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 醋酸与氢氧化钠反应:H++OH-═H2O | |
| B. | 稀硫酸与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO${\;}_{4}^{2-}$═BaSO4↓ | |
| D. | 碳酸钠与盐酸反应:CO${\;}_{3}^{2-}$+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com