


科目:高中化学 来源:不详 题型:单选题
 2CO2+4H2O。下列关于该电池的分析:①甲醇是负极②H+向负极移动③负极反应:CH3OH-6e-+H2O=CO2+6H+ ④1 mol CH3OH完全反应转移12 mol电子 ⑤正极反应:O2+4e-+2H2O==4OH-⑥该电池的电解质溶液可能是碱液。其中正确的是
2CO2+4H2O。下列关于该电池的分析:①甲醇是负极②H+向负极移动③负极反应:CH3OH-6e-+H2O=CO2+6H+ ④1 mol CH3OH完全反应转移12 mol电子 ⑤正极反应:O2+4e-+2H2O==4OH-⑥该电池的电解质溶液可能是碱液。其中正确的是| A.①②⑥ | B.②③④⑤ | C.③ | D.①③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
B.下图中电子由Zn极流向Cu,盐桥中的Cl-移向CuSO4溶液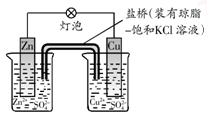 |
| C.氢氧燃料电池(酸性电解质)中O2通入正极,电极反应为O2+4H+ +4e-=2H2O |
| D.电镀时,通常把待镀的金属制品作阳极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
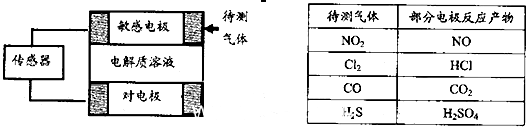
| A.上述气体检测时,敏感电极均作电池正极 |
B.检测Cl2气体时,敏感电极的电极反应为: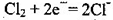 |
C.检测H2S气体时,对屯极充入空气,对电极上的电极反应式为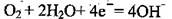 |
| D.检测H2S和CO体积分数相同的两份空气样本时,传感器上产生的电流大小相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
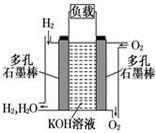
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| B.用锌片做阳极,铁片做阴极,电解氯化锌溶液,铁片表面出现一层锌 |
| C.把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |
| D.把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在氧化还原反应中,甲原子失去的电子比乙原子失去的电子多 |
| B.同价态的阳离子,甲比乙的氧化性强 |
| C.甲能跟稀盐酸反应放出氢气而乙不能 |
| D.将甲、乙作电极组成原电池时,甲是正极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。
LiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含Li+导电固体为电解质。| A.可加入硫酸以提高电解质的导电性 | B.放电时Li+向负极移动 |
| C.充电过程中,电池正极材料的质量减少 | D.放电时电池正极反应为:Li-e-=== Li+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、C(石墨) | 稀盐酸 | 偏向石墨 |
| 4 | Mg、Al | 氢氧化钠溶液 | 偏向Mg |
| 5 | Al、Zn | 浓硝酸 | 偏向Al |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com