
| A.Na+、Ba2+、S2-、SO42- | B.H+、K+、SO32-、SO42- |
| C.Fe2+、H+、ClO-、S2- | D.K+、NH4+、SO42-、NO3- |
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源:不详 题型:填空题
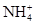 、Cl-
、Cl- 、
、 ,现取两份100 mL溶液进行如下实验:①第一份加过量NaOH溶液加热后,只收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。②在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g。③第二份加足量BaCl2溶液后,得白色沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65 g。根据上述实验回答:
,现取两份100 mL溶液进行如下实验:①第一份加过量NaOH溶液加热后,只收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。②在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g。③第二份加足量BaCl2溶液后,得白色沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65 g。根据上述实验回答:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 阳离子 | Ag+ Na+ Fe3+ Al3+ Ba2+ |
| 阴离子 | OH- Cl- SO32— NO SO42— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 物质 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe(OH)3 | 2.2 | 3.2 |
| Fe(OH)2 | 7.6 | 9.6 |
| Cu(OH)2 | 4.7 | 6.4 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cl-、Br-、I- | B.I-、Br-、 Cl- |
| C.Br-、 Cl-、I- | D.Br-、I-、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Mg、AlCl3、NaAlO2 | B.KNO3、NaCl、CH3COONa |
| C.NaClO、Na2SO3、BaCl2 | D.Ba(NO3)2、FeSO4、NH4HCO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com