
【题目】判断下列有关化学基本概念的依据正确的是
A.溶液与浊液:不同的本质原因是是否为无色透明
B.纯净物与混合物:是否仅含有一种元素
C.氧化还原反应:元素化合价是否变化
D.电解质与非电解质:物质本身的导电性
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】在锌和稀硫酸制氢气的反应中,要使反应速率加快应采取的措施是( )
A. 加入少量硫酸钠溶液 B. 加入少量氯化锌溶液
C. 把纯锌换成有杂质的锌 D. 把稀硫酸换成浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用。下表列出了12种元素在周期表中的位置。
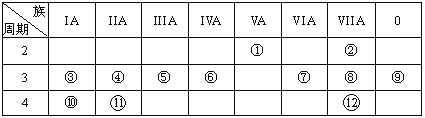
请回答:
(1)写出下列元素符号:①________,⑥________,⑦________。
(2)在①~12元素中,金属性最强的元素是________,非金属性最强的元素是________,最不活泼的元素是________。(均填元素符号)
(3)元素⑦与元素⑧相比,非金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是________。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题:
周期\族 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)⑤、⑥、⑦的原子半径由大到小的顺序为_________________(填元素符号)。它们的最高价氧化物对应水化物的碱性从强到弱的顺序为______________(填最高价氧化物对应水化物的化学式)。
(2)②、⑧、⑨的最高价含氧酸的酸性由强到弱的顺序是__________________(填最高价含氧酸的化学式)。
(3)①、④、⑤三种元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:__________________。
(4)由表中①、④两种元素的原子可按1∶1组成的一种常见液态化合物。此液态化合物的电子式为:__________________。请写出此液态化合物在MnO2催化作用下分解的化学方程式____________
(5)⑧是极好的半导体材料,而且能与③在高温的条件下生成一种优良的新型陶瓷材料,请写出这个反应的化学方程式:__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,按化合物、单质、混合物的顺序排列的是( )
A.干冰、铁、氯化氢
B.生石灰、白磷、熟石灰
C.烧碱、液态氧、碘酒
D.空气、氮气、胆矾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】冷冻显微术是一种研究生物大分子结构的新方法,瑞士、美国和英国科学家因此分获了2017年诺贝尔化学奖。下列属于生物大分子的是
A. 葡萄糖 B. 植物油 C. 聚乙烯 D. 蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体区别于其它分散系的本质特征是
A.胶体是纯净物,其它分散系是混合物 B.胶体能产生丁达尔现象
C.胶体的分散质粒子直径在1~100nm之间 D.胶体的分散质能透过滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、硅两元素广泛存在于自然界中.请回答下列问题:
(1)基态14C原子的核外存在________对自旋方向相反的电子,硅原子的电子排布式为__________。
(2)晶体硅的结构与全刚石非常相似。晶体硅硅中硅原子的杂化方式为_______杂化;金刚石、晶体硅和金刚砂(碳化硅)的熔点由高到低的顺序为_____________。
(3)科学研究结果表明,碳的氧化物CO2能够与H2O借助子太阳能制备HCOOH。其反应原理如下:2CO2+2H2O=2HCOOH+O2,则生成的HCOOH分子中δ键和π键的个数比是_______。
(4)碳单质有多种形式,其中C60、石墨烯与金刚石晶体结构如图所示:

①C60、石墨烯与金刚石互为_________。
②C60形成的晶体是分子晶体,C60分子中含有12个五边形和20个六边形,碳与碳之间既有单键又有双键,已知C60分子所含的双键数为30,则C60分子中_______个C—C 键(多面体的顶点数、面数和棱边数的关系,遵循欧拉定理:顶点数+面数-棱边数=2)。在石墨烯晶体中,每个C原子连接______个六元环;在金刚石晶体中,每个C原子连接的最小环也为六元环,六元环屮最多有_______个C原子在同一平面。
③金刚石晶胞含有______个碳原子。若碳原子的半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=______a,列式表示碳原子在晶胞中的空间占有率为_______(不要求计算结果)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com