
【题目】镁条在空气中燃烧时,镁可与空气中的一种主要成分反应,生成少量的物质A,已知A有下面一系列变化。气体C能够使湿润的红色石蕊试纸变蓝。
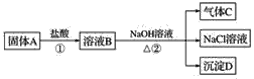
(1)写出A、C、D的化学式:
A________;C________;D________。
(2)写出下列反应的化学方程式:
①______________________________________________;
②____________________________________________。
【答案】Mg3N2 NH3 Mg(OH)2 Mg3N2+8HCl=3MgCl2+2NH4Cl MgCl2+2NaOH=Mg(OH)2↓+2NaCl,NH4Cl+NaOH![]() NaCl+H2O+NH3↑
NaCl+H2O+NH3↑
【解析】
镁条在空气中燃烧时,镁可与空气中的一种主要成分反应,镁和空气生成氧化镁和氮化镁,生成少量的物质A,即A为氮化镁,气体C能够使湿润的红色石蕊试纸变蓝,说明C为氨气。溶液B为氯化铵和氯化镁的混合,溶液B于氢氧化钠反应生成氢氧化镁沉淀、氨气和氯化钠。
(1)根据上面分析得出A、C、D的化学式:A为Mg3N2;C为NH3;D为Mg(OH)2,故答案为:Mg3N2;NH3;Mg(OH)2。
(2)①氮化镁和盐酸反应生成氯化镁和氯化铵,反应方程式为Mg3N2+8HCl=3MgCl2+2NH4Cl,故答案为:Mg3N2+8HCl=3MgCl2+2NH4Cl。
②氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,反应方程式为MgCl2+2NaOH=Mg(OH)2↓+2NaCl,氯化铵和氢氧化钠加热反应生成氯化钠、氨气和水,反应方程式为NH4Cl+NaOH![]() NaCl+H2O+NH3↑,故答案为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl,NH4Cl+NaOH
NaCl+H2O+NH3↑,故答案为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl,NH4Cl+NaOH![]() NaCl+H2O+NH3↑。
NaCl+H2O+NH3↑。


科目:高中化学 来源: 题型:
【题目】“笔、墨、纸、砚”在中国传统文化中被称为“文房四宝”,下列说法中错误的是( )
A.羊毫笔笔头用山羊毛制成,用灼烧法可鉴别羊毫和化纤
B.“松烟墨”以松树烧取的烟灰制成,用此墨写字日久会褪色
C.制作宣纸的原料有青檀树皮和稻草,其主要成分均是纤维素
D.端砚石主要成分含水白云母![]() ,它属于硅酸盐
,它属于硅酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1L0.1mol·L-1一元酸HR溶液中逐渐通入氨气[已知常温下NH3·H2O电离平衡常数K=1.76×10-5],使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
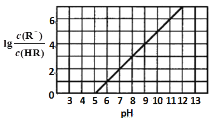
A.0.1mol·L-1HR溶液的pH为5
B.当pH=6时,水电离出的氢离子浓度为1.0×10-6
C.当通入0.1 mol NH3时,c(![]() )>c(R-)>c(H+)>c(OH-)
)>c(R-)>c(H+)>c(OH-)
D.当 pH=7时,c(![]() )=c(R-)
)=c(R-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烷燃烧可以通过以下两种途径:
途径I:C3H8(g) + 5O2(g) == 3CO2(g) +4H2O(l) ΔH=-a kJ·mol-1
途径II:C3H8(g) ==C3H6(g)+ H2(g) ΔH=+b kJ·mol-1
2C3H6(g)+ 9O2(g) == 6CO2(g) +6H2O(l) ΔH=-c kJ·mol-1
2H2(g)+O2(g) == 2H2O(l) ΔH=-d kJ·mol-1(a、b、c、d均为正值)
请回答下列问题:
(1)判断等量的丙烷通过两种途径放出的热量,途径I放出的热量 ______(填“大于”、“等于”或“小于”)途径II放出的热量。
(2)由于C3H8(g) ==C3H6(g)+ H2(g) 的反应中,反应物具有的总能量______(填“大于”、“等于”或“小于”)生成物具有的总能量,那么在化学反应时。反应物就需要______(填“放出”、或“吸收”)能量才能转化为生成物,因此其反应条件是______________。
(3)b 与a、c、d的数学关系式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】给定条件下,下列选项中所示的物质间转化均能一步实现的是( )
A. 粗硅![]() SiCl4
SiCl4![]() Si
Si
B. Mg(OH)2![]() MgCl2(aq)
MgCl2(aq)![]() Mg
Mg
C. Fe2O3![]() FeCl3(aq)
FeCl3(aq)![]() 无水FeCl3
无水FeCl3
D. AgNO3(aq)![]() [Ag(NH3)2]OH(aq)
[Ag(NH3)2]OH(aq)![]() Ag
Ag
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题:
(1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下:
①C4H10(g)= C4H8(g)+H2(g) ΔH1
已知:②C4H10(g)+ ![]() O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
O2(g)= C4H8(g)+H2O(g) ΔH2=-119 kJ·mol-1
③H2(g)+ ![]() O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
O2(g)= H2O(g) ΔH3=-242 kJ·mol-1
反应①的ΔH1为________ kJ·mol-1。图(a)是反应①平衡转化率与反应温度及压强的关系图,x_____________0.1(填“大于”或“小于”);欲使丁烯的平衡产率提高,应采取的措施是__________(填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强
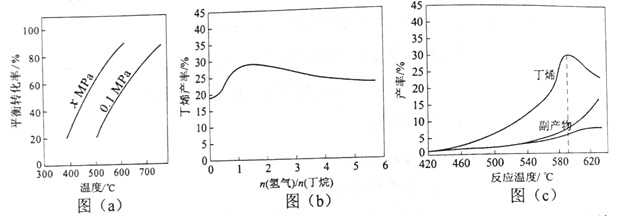
(2)丁烷和氢气的混合气体以一定流速通过填充有催化剂的反应器(氢气的作用是活化催化剂),出口气中含有丁烯、丁烷、氢气等。图(b)为丁烯产率与进料气中n(氢气)/n(丁烷)的关系。图中曲线呈现先升高后降低的变化趋势,其降低的原因是___________。
(3)图(c)为反应产率和反应温度的关系曲线,副产物主要是高温裂解生成的短碳链烃类化合物。丁烯产率在590℃之前随温度升高而增大的原因可能是___________、____________;590℃之后,丁烯产率快速降低的主要原因可能是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入150 mL 4 mol·L-1的稀硝酸恰好使混合物完全溶解,放出2.24 L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现。若用足量的H2在加热条件下还原相同质量的混合物,所得到的铁的物质的量为( )
A. 0.21 mol B. 0.25 mol C. 0.3 mol D. 0.35 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积固定的密闭容器中,加入2molA和1molB发生下列反应并且达到化学平衡状态,2A(g)+B(g) ![]() 3C(g)+D(g),平衡时C的浓度为amol·L-1。若维持容器体积和温度不变,按下列4种方法配比作为起始物质充入该容器中,达到平衡后,C的浓度仍为amol·L-1的是( )
3C(g)+D(g),平衡时C的浓度为amol·L-1。若维持容器体积和温度不变,按下列4种方法配比作为起始物质充入该容器中,达到平衡后,C的浓度仍为amol·L-1的是( )
A.4molA+2molB B.3molC+1molB+1molD+1molA
C.2molA+1molB+1molD D.1molA+0.5molB + 1.5molC+0.5molD
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,有质量相同的CO2、H2、O2、CH4、SO2五种气体,下列有关说法错误的是( )
A.气体的体积由大到小的顺序是H2>CH4>O2>CO2>SO2
B.所含分子数由多到少的顺序是H2>CH4>O2>CO2>SO2
C.密度由大到小的顺序是SO2>CO2>O2>CH4>H2
D.所含电子数由多到少的顺序是CO2>SO2>CH4>O2>H2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com