
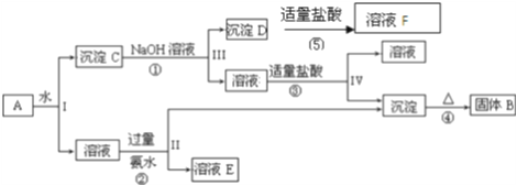
����Ŀ��ij�����A����KAl��SO4��2��Al2O3��Fe2O3����һ�������¿�ʵ����ͼ��ʾ������֮��ı仯��
�ݴ˻ش��������⣺
��1��I��II��III��IV�IJ��ж�����Һ�ͳ����ķ����ȡ�ķ�����_____________��
��2������������ͼ��Ӧ��ϵ��д������B��D�������ʵĻ�ѧʽ��
����B_____________������D_______________��
��3��д���ٷ�Ӧ�Ļ�ѧ����ʽ__________��
��4��д���ڡ���������Ӧ�����ӷ���ʽ
��__________________________����______________��
��5�����ʵ�������ҺF���������ʣ�_______________��
��6���ֱ�д������B�ͳ���D�ڹ�ҵ�ϵ�һ����Ҫ��;��
����B��______________________������D��_______________________��
���𰸡����� Al2O3 Fe2O3 Al2O3��2OH��=2AlO2����H2O Al3����3NH3��H2O=Al(OH)3����3NH4�� AlO2����H����H2O=Al(OH)3�� ȡF��Һ��������֧�Թ��У�һ֧�еμ�KSCN��Һ������Ѫ��ɫ֤��F��Һ�к���Fe3��������һ֧�Թ��м���ϡ�����ữ��Ȼ���ټ�����������Һ�����а�ɫ�������ɣ�֤��F��Һ����Cl�� ұ���� �ͻ���� ����ԭ�� ��ɫ���� Ϳ��
��������
�����̿�֪��Al2O3��Fe2O3������ˮ�������CΪAl2O3��Fe2O3������������Ӧ�������DΪFe2O3����Ӧ�ڢ������ɵij���ΪAl(OH)3�����ȷֽ�����BΪAl2O3����Ӧ��ΪKAl(SO4)2����ˮ�ķ�Ӧ������ҺEΪK2SO4��(NH4)2SO4��NH3.H2O��������������֪��BΪAl2O3��DΪFe2O3��EΪK2SO4��(NH4)2SO4��NH3.H2O��
��1�����IJ��ж�����Һ�ͳ����ķ��뷽��Ϊ���ˣ�
�ʴ�Ϊ�����ˣ�
��2������������ͼ��Ӧ��ϵ���������̹���BΪAl2O3������DΪFe2O3��
����Al2O3 �� Fe2O3
��3���ٷ�ӦΪ���������������Ʒ�Ӧ����ƫ�����ƺ�ˮ����ѧ����ʽAl2O3��2OH��=2AlO2����H2O��
����Al2O3��2OH��=2AlO2����H2O��
��4����Ӧ��Ϊ�������백ˮ��Ӧ������������������笠����ӣ����ӷ�ӦΪAl3����3NH3��H2O=Al(OH)3����3NH4������Ӧ��ƫ����������������ӷ�Ӧ���������������������ӷ�ӦΪAlO2����H����H2O=Al(OH)3����
��5�������������ᷴӦ�����Ȼ�����ˮ����ҺF����Ҫ�������������Ӻ������ӣ����������Ӻ������ӵIJ���ΪȡF��Һ��������֧�Թ��У�һ֧�еμ�KSCN��Һ������Ѫ��ɫ֤��F��Һ�к���Fe3��������һ֧�Թ��м���ϡ�����ữ��Ȼ���ټ�����������Һ�����а�ɫ�������ɣ�֤��F��Һ����Cl�� ��
��Ϊ��ȡF��Һ��������֧�Թ��У�һ֧�еμ�KSCN��Һ������Ѫ��ɫ֤��F��Һ�к���Fe3��������һ֧�Թ��м���ϡ�����ữ��Ȼ���ټ�����������Һ�����а�ɫ�������ɣ�֤��F��Һ����Cl�� ��
��6���ֱ�д������B�ͳ���D�ڹ�ҵ�ϵ�һ����Ҫ��;��
����BΪ����������ҵ���õ�������������ķ�����ұ�������������������۵�ܸߣ������������ͻ���ϣ�����DΪ�������������׳����죬���������������Ϳ�ϣ���ҵ����Ϊұ������ԭ�ϡ�
��Ϊ��ұ���� �ͻ���ϣ�����ԭ�� ��ɫ���� Ϳ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������һ����������ű����ҩ������ȫ���ر��Ƿ�չ�й��ҵ��������˵����������ķ���ʽΪC15H22O5�����������ص�˵����ȷ���ǣ� ��
A.2.82g�����غ���ԭ����ĿΪ0.05NA
B.��״���£�1 mol�����ص����Ϊ22.4 L
C.�����غ�������������Ϊ10%
D.�����ص�Ħ������Ϊ282
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�����û�������ˮ�ķ����ϳɻ���ϩ����ʵ���װ������ͼ��ʾ��

�����õ����й��������£�
��Է������� | �ܶȣ�(g��cm-3) | �е㣯�� | �ܽ��� | |
���Ѵ� | 100 | 0.9618 | 161 | ����ˮ |
����ϩ | 82 | 0.8102 | 83 | ������ˮ |
������ʵ�鲽��ش����⣺
��������ϳ�
��a�м���10.0g��������2Ƭ���Ƭ����ȴ��������������1mLŨ���ᣬb��ͨ����ȴˮ��ʼ��������a�������������¶Ƚӽ�90����
��l�����Ƭ��������________��b��������________��
��2��a�з�����Ҫ��Ӧ�Ļ�ѧ����ʽΪ____________________________����ʵ�������ײ������л�������Ľṹ��ʽΪ________��
���������ᴿ
����Ӧ�ֲ��ﵹ���Һ©���У�����������5%̼������Һ��ˮϴ�ӣ�����������ˮ�Ȼ��ƿ���������һ��ʱ�����ȥ�Ȼ��ƣ�����ͨ������X�õ������Ļ���ϩ��������������Ϊ4.1g��
��3����̼������Һϴ�ӵ�������________������X������Ϊ________��
����������������ʼ���
��4���ٺ˴Ź��������������������Ƿ�Ϊ����ϩ������ϩ��������_______�ֲ�ͬ��ѧ��������ԭ�ӡ�
�� ��ʵ�����û���ϩ�IJ�����_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȫ������Ϊ�����ı��䣬��Ϊ��������������ײʱ����ȫ������Ѹ�ٷ�����Ӧ��10NaN3+2KNO3=K2O+5Na2O+16N2������������������ʹ����Ѹ�ٵ��������ϼݳ˳���Ա��ȫ�����й��ڸ÷�Ӧ��˵����ȷ����
A.�÷�Ӧ��NaN3����������KNO3�ǻ�ԭ��
B.���������뻹ԭ��������ʵ���֮��Ϊ1��15
C.����50.5 g KNO3�μӷ�Ӧ������0.5mol Nԭ�ӱ���ԭ
D.ÿת��1 mol e�������ɱ�״����N2�����Ϊ2.24 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
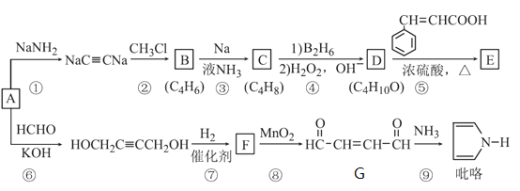
����Ŀ����A��C2H2��Ϊԭ�Ϻϳ�ʳ������E��������pyrrole����·����ͼ��ʾ�����ַ�Ӧ������������ȥ������D��һ�������¿ɱ�������ͪ��
�ش��������⣺
��1��A������������_______________��C��������_______________��
��2���ķ�Ӧ������_______________����ķ�Ӧ������_______________��
��3����Ӧ�ݵĻ�ѧ����ʽΪ____________________________��
��4��������������������ᣨ![]() ����ͬ���칹�干��_________�֣������������칹��:�ٺ��б��� ������������Ȼ�̼��Һ��ɫ ����ˮ�⡣��G��Ϊͬ���칹�壬�Һ˴Ź�������ֻ��һ�����л���Ľṹ��ʽ��________������дһ�֣�
����ͬ���칹�干��_________�֣������������칹��:�ٺ��б��� ������������Ȼ�̼��Һ��ɫ ����ˮ�⡣��G��Ϊͬ���칹�壬�Һ˴Ź�������ֻ��һ�����л���Ľṹ��ʽ��________������дһ�֣�
��6�����������ϳ�·�ߣ����һ����A����ȩΪ��ʼԭ���Ʊ�2,5-����������![]() ���ĺϳ�·��_________________________________��
���ĺϳ�·��_________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶�ΪTʱ����2.0L�����ܱ������г���1.0 mol PCl5����ӦPCl5(g)![]() PCl3(g)��Cl2(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ����
PCl3(g)��Cl2(g)��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ�IJ������ݼ��±�������˵����ȷ����
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A����Ӧ��ǰ50 s��ƽ������Ϊv(PCl3)=0.0032mol��L��1��s��1
B�����������������䣬�����¶ȣ�ƽ��ʱc(PCl3)=0.11mol��L��1����Ӧ����H��0
C����ͬ�¶��£���ʼʱ�������г���1.0mol PCl5��0.20mol PCl3��0.20molCl2���ﵽƽ��ǰv(��)��v(��)
D����ͬ�¶��£���ʼʱ�������г���2.0mol PCl3��2.0molCl2���ﵽƽ��ʱ��PCl3��ת����С��80%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪2Mg+CO2![]() 2MgO+C,ijͬѧ�Ʋ�����CO2Ҳ�ܷ�Ӧ��Ϊ̽����Ӧ���������ͼװ�ý���ʵ�顣(��֪PdCl2�ܱ�CO��ԭΪ��ɫ��Pd,����NaHCO3��Һ�������ڳ�ȥCO2 �е�HC1����)
2MgO+C,ijͬѧ�Ʋ�����CO2Ҳ�ܷ�Ӧ��Ϊ̽����Ӧ���������ͼװ�ý���ʵ�顣(��֪PdCl2�ܱ�CO��ԭΪ��ɫ��Pd,����NaHCO3��Һ�������ڳ�ȥCO2 �е�HC1����)
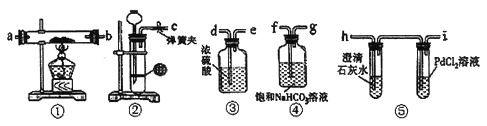
��1��װ�â�����ϡ������CaCO3��Ӧ�Ʊ�CO2,�Ʊ�������ʱ������Ӧ�����ӷ���ʽ��______��
��2���뽫ͼ�и�װ�ð�˳������(���b�ýӿ���ĸ): c��____��____��____��____��____��_____��______��
��3��װ�â۵�������_____��
��4�������װ�������Բ�װ��ҩƷ��ȼ�ƾ���֮ǰӦ���еIJ����Ǵ��ɼУ���CO2��������װ�ã����۲쵽________ʱ�ٵ�ȼ�ƾ��ơ��˲�������Ŀ����______��
��5����������ʵ�������ƲⲢ��д������CO2��Ӧ�Ļ�ѧ����ʽ��
I.ʵ����������۲쵽װ�â�PdCl2��Һ���к�ɫ��������װ�â��й���ɷ�ֻ��һ�֣�������м���ϡ����ɲ�����ʹ����ʯ��ˮ���������塣��д������CO2��Ӧ�Ļ�ѧ����ʽ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
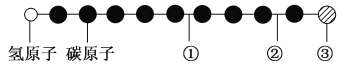
����Ŀ���ݱ�����������������һ���µ��Ǽʷ��ӣ������ģ����ͼ��ʾ(ͼ��������֮������ߴ�����ѧ�����絥����˫���������ȣ���ɫ��ͬ�����ʾͬһ��ԭ��)��
���жԸ����ʵ�˵������ȷ����
A. �ٴ��Ļ�ѧ����ʾ̼̼˫�� B. �ڴ��Ļ�ѧ����ʾ̼̼����
C. �۴���ԭ�ӿ�������ԭ�ӻ��ԭ�� D. ���Ǽʷ�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��д����ͼ����Ţ١������������ƣ�
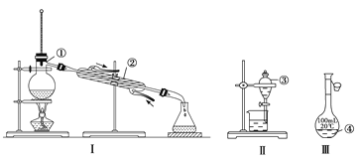
��_____________����__________�� ��_____________�� ��____________��
��2�������١����У�ʹ��ʱ�������Ƿ�©ˮ����__________����������ţ���
��3����ͼ��ijѧУʵ���Ҵӻ�ѧ�Լ��̵���ص�Ũ�����Լ���ǩ�ϵIJ������ݡ����ø�Ũ��������480 mL 1 mol��L��l��ϡ���ᡣ

�ɹ�ѡ�õ������У� �ٽ�ͷ�ιܣ�����ƿ�����ձ�����ҩ�ף�����Ͳ����������ƽ����ش��������⣺
������ϡ����ʱ����ȱ�ٵ�������____________��___________��д�������ƣ���
�ھ����㣬����480 mL l mol��L��l��ϡ������Ҫ����Ͳ��ȡ����Ũ��������Ϊ_______mL��
����ת������ƿǰ�ձ���Һ��Ӧ____________�������ʹ���Ũ��___________������ƫ������ƫ����������Ӱ��������
�ܶ���ʱ����ʹ��Һ�İ�Һ����̶�����ƽ�������ӻ�ʹŨ��_________��������ƫ������ƫ����������Ӱ��������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com