
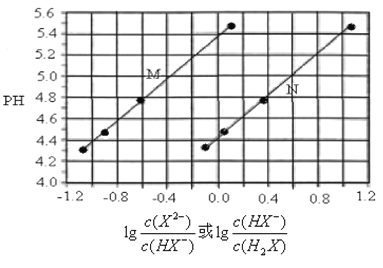
【题目】常温下将KOH溶液滴加到己二酸(H2X) 溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
A. Ka2(H2X)的数量级为10–4
B. KHX溶液中c(H+)>c(OH-)
C. 曲线N表示pH与1g[c(X2-)/c(HX-)]的变化关系
D. 当混合溶液呈中性时,c(K+) >c(HX-) > c(X2-) > c(OH-) =c(H+)
【答案】B
【解析】H2X为二元弱酸,以第一步电离为主,则Ka1(H2X)>Ka2(H2X),酸性条件下,则pH相同时c(HX)/ c(H2X)>c(X2-)/c(HX-),由图像可知N为lg[c(HX)/ c(H2X)]的变化曲线,M为lg[c(X2-)/c(HX-)]的变化曲线,当lg[c(HX)/ c(H2X)]或lg[c(X2-)/c(HX-)]=0时,说明[c(HX)/ c(H2X)]或[c(X2-)/c(HX-)]=1,浓度相等。A.lg[c(X2-)/c(HX-)]=0时,c(X2-)/c(HX-)=1,此时pH≈5.4,则Ka2(H2X)≈10-5.4,可知Ka2(H2X)的数量级为10-6,故A错误;B.由图像可知,lg[c(X2-)/c(HX-)]=0时,即c(HX-)=c(X2-),此时pH≈5.4,可知HX-电离程度大于X2-水解程度,溶液显酸性,则NaHX溶液呈酸性,溶液中c(H+)>c(OH-),故B正确;C.由以上分析可知曲线N表示pH与lg[c(HX)/ c(H2X)]的变化关系,故C错误;D.由图像可知当pH=7时,lg[c(X2-)/c(HX-)]>0,则c(X2-)>c(HX-),所以溶液中存在:c(Na+)>c(X2-)>c(HX-)>c(H+),故D错误;故选B。


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 实验室应将钠保存在煤油中
B. 分液漏斗和容量瓶在使用前都要检漏
C. 可用酒精代替CCl4萃取碘水中的碘单质
D. 金属镁失火不可用水来灭火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知: A、B、C、D、E、F、G 是原子序数依次增大的短周期主族元素,A的原子核内无中子,B、F 在元素周期表中的相对位置如图,B 与D 能形成两种无色气体,D 是地壳中含量最多的元素,E是地壳中含量最多的金属元素;

请回答下列问题:
(1)BF2 的结构式为:_____________;
(2)D和F的简单氢化物中沸点较高的是:________。(填化学式)
(3)实验室制取G2气体的离子方程式为:____________________;
(4)在微电子工业中,C 的最简单气态氛化物的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物 不污染环境,其化学方程式为:___________________;
(5)FD2 气休通入BaCl2 和C的最高价氧化物对应的水化物的混合溶液中,生成白色沉淀和无色气体, 有关反应的离子方程式为_____________________;
(6)火箭使用B2A8C2 作燃料,N2O4为氧化剂,燃烧放出的巨大能量能把火箭送入太空,并且产生三种 无污染的气体,其化学方程式为:_________________;
(7)上述元索可组成盐Q: CA4E(FD4)2。向盛有20 mL 0.5 mol/L Q溶液的烧杯中加入12 mL2.0 mo/LBa(OH)2溶液,充分反应后,溶液中产生沉定的物质的量为:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写不正确的是
A. 盐酸与Na2SiO3溶液混合: SiO32-+2H+=H2SiO3↓
B. 浓盐酸和二氧化锰共热制取Cl2: MnO2+4H++2Cl- ![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
C. NO2通入水中: H2O+3NO2=2H++2NO3-+NO
D. 向澄清石灰水中通人过量SO2: SO2+Ca2++2OH-=CaSO4↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素在元素周期表中的位置关系如右表所示。
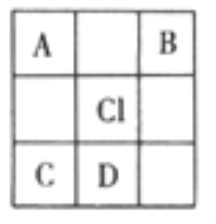
(1)A的最简单氢化物的化学式为_________
(2)B的原子结构示意图为__________
(3)C 的原子序数为_________
(4)D的单质与KI反应的离子方程式为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)相同条件下,体积之比为a:b和质量之比为a:b的H2和O2的混合气体,其平均相对分子质量为和 .
(2)已知各物质参加反应的物质的量之比等于其在化学方程式中的计量数之比,气体化合物A的分子式可表示为OxFy , 同温同压下,10mLA受热分解生成15mLO2和10mLF2 , 则A的化学式为 , 推断的依据为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分:
碳 | 氮 | Y | |
X | 硫 | Z |
请回答下列问题:
(1)Z元素在周期表中的位置为________________。
(2)表中元素原子半径最大的是(写元素符号)________________。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是________(填序号)。
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1mol硫得电子多
c.Y和硫两元素的简单氢化物受热分解,前者的分解温度高
(4)现有一定量的铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L2.2mol·L-1 NaOH溶液和1molO2,则两种气体的分子式及物质的量分别为______________________________,生成硫酸铜物质的量为_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应一定能用H++OH-=H2O表示的化学方程式有( )
A. 氢氧化钠溶液与醋酸反应 B. 氢氧化钙与稀盐酸反应
C. 氢氧化钡与稀硫酸反应 D. 氢氧化钾与稀硝酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】很多鲜花和水果的香味都来自酯的混合物.如图,图1是乙烯等为原料制取乙酸乙酯的过程(部分产物和反应条件已略去). 
请回答下列问题:
(1)B的结构简式为 .
(2)乙烯与水反应生成A的反应类型为 .
(3)A与C反应生成乙酸乙酯的化学方程式为 , 其反应类型为 .
(4)实验室可用图2装置制取乙酸乙酯. ①在试管a中加好相关试剂后,还需要加入2﹣3块的碎瓷片,其作用是 .
②试管b中盛有饱和碳酸钠溶液,生成的乙酸乙酯在该溶液的(填“上”或“下”)层,用分液的方法分离出该产品所需的主要仪器是 . 试管b中的导管口应在液面上方而不伸入到液面以下,其原因是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com