
【题目】下列关于有机化合物的说法正确的是( )
A.![]() 的名称为2﹣甲基﹣1﹣丙醇
的名称为2﹣甲基﹣1﹣丙醇
B.氯乙烯和聚乙烯均能发生加成反应
C.C3H2Cl6 有4种同分异构体
D.C2H4和C4H8一定是同系物
【答案】C
【解析】解:A. ![]() 含有羟基的最长碳链为4,在2号碳上含有羟基,立强基近的一端编号得到名称为2﹣丁醇,故A错误;
含有羟基的最长碳链为4,在2号碳上含有羟基,立强基近的一端编号得到名称为2﹣丁醇,故A错误;
B.氯乙烯能发生加成反应,聚乙烯不能发生加成反应,故B错误;
C.分子式为C3H2Cl6的有机物可以看作C3Cl8中的两个Cl原子被两个H原子取代,
碳链上的3个碳中,两个氢原子取代一个碳上的氯原子,有两种,CCl3﹣CCl2﹣CClH2 、CCl3﹣CH2 ﹣CCl3;
分别取代两个碳上的氯原子,有两种:CCl2H﹣CCl2﹣CCl2H(两个边上的),CCl2H﹣CHCl﹣CCl3 (一中间一边上),故C3H2Cl6共有四种,故C正确;
D.C2H4和C4H8不一定是同系物,C4H8可以是丁烯也可以是环丁烷,结构不相似,故D错误;
故选C.


科目:高中化学 来源: 题型:
【题目】某校研究性学习小组用一些大部分已经锈蚀(成分为 Fe2O3)的废铁屑制备绿矾(FeSO4·7H2O),实验操作过程如下:

已知:杂质不溶于稀硫酸。
请回答下列问题:
(1)步骤①中,稀硫酸与 Fe2O3反应的离子方程式为 ______,废铁屑用硫酸处理后,还含有不溶性杂质,为获取澄清的A溶液,需进行的操作名称是 _________。
(2)步骤②中溶液A与铁粉反应的离子方程式为________________。
(3)检验溶液 B 中是否还存在杂质金属阳离子的方法是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在用稀硫酸与锌制取氢气的实验中,发现反应条件不同,反应速率不同。请回答下列问题:
(1)在用稀硫酸与锌制氢的实验中,加入少量下列物质可加快氢气生成速率的是_____(填序号)
A.Na2SO4 溶液 B.MgSO4 溶液 C.SO3 D.CuSO4 溶液
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列的实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。
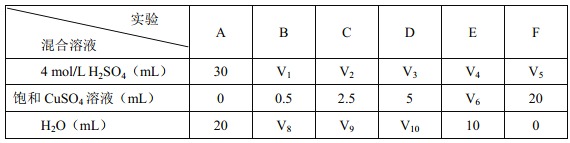
请完成此实验设计,其中:V1=____ mL, V6=______ mL。
该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析速率下降的主要原因__________ 。
(3)该同学为探究其它因素对锌与稀硫酸反应速率的影响,又做了以下实验,记录数据如下,回答下列问题:
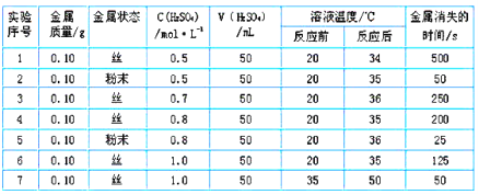
①由实验可推知,反应物的总能量_______产物的总能量(填“<”、 “>” 或“=”)。
②实验2和5表明,______对反应速率有影响。
③实验4和5表明,______对反应速率有影响,能表明同一规律的实验还有 _________ (填实验序号)。
④本实验中影响反应速率的其他因素还有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知:|||+ ![]()
![]()
![]() ,如果要合成
,如果要合成 ![]() ,所用的起始原料可以是( ) ①2﹣甲基﹣1,3﹣丁二烯和2﹣丁炔
,所用的起始原料可以是( ) ①2﹣甲基﹣1,3﹣丁二烯和2﹣丁炔
②1,3﹣戊二烯和2﹣丁炔
③2,3﹣二甲基﹣1,3﹣戊二烯和乙炔
④2,3﹣二甲基﹣1,3﹣丁二烯和丙炔.
A.①④
B.②③
C.①③
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
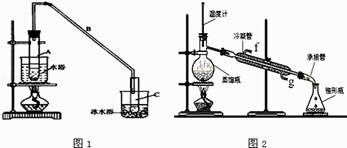
【题目】某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯 已知: 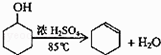
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)制备粗品将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品. ①A中碎瓷片的作用是 , 导管B除了导气外还具有的作用是 .
②试管C置于冰水浴中的目的是 .
(2)制备精品 ①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静置、分层,环己烯在层(填上或下),分液后用(填入编号)洗涤.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图2所示装置蒸馏,冷却水从口进入,目的是 .
③收集产品时,控制的温度应在左右,实验制得的环己烯精品质量低于理论产量,可能的原因是
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是 . a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①H2O(g)═H2O(l)△H1=﹣Q1 kJmol﹣1②CH3OH(g)═CH3OH(l)△H2=﹣Q2 kJmol﹣1
③2CH3OH(g)+3O2(g)═2CO2(g)+4H2O(g)△H3=﹣Q3 kJmol﹣1(Q1、Q2、Q3均大于0)
若要使32g液态甲醇完全燃烧,最后恢复到室温,放出的热量为(单位:kJ)( )
A.Q1+Q2+Q3
B.0.5Q3﹣Q2+2Q1
C.0.5Q3+Q2﹣2Q1
D.0.5(Q1+Q2+Q3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2和N2O4可以相互转化:2NO2(g)N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如图.下列说法错误的是( ) 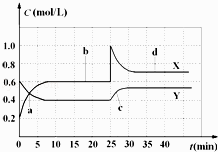
A.图中共有两条曲线X和Y,其中曲线X表示NO2浓度随时间的变化
B.a、b、c、d四个点中,表示化学反应处于平衡状态的点是b和d
C.反应进行至25min时,曲线发生变化的原因是加入0.4mol N2O4
D.若要达到与d相同的状态,在25min时还可以采取的措施是适当缩小容器体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com