
下列是除去括号内杂质的有关操作,其中正确的是
A.苯(己烷):分液
B.NO(NO2):通过水洗、干燥后,用向下排空气法收集
C.乙烷(乙烯):让气体通过盛酸性高锰酸钾溶液的洗气瓶
D.乙醇(乙酸):加足量NaOH溶液,蒸馏
科目:高中化学 来源: 题型:
氨气具有广泛的用途。
(1)工业上合成氨反应的化学方程式是 。
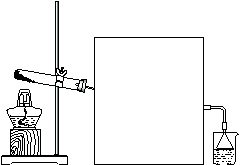 (2)实验室常用如下图所示装置制取并收集氨气。
(2)实验室常用如下图所示装置制取并收集氨气。
 |
① 实验室制取氨气反应的化学方程式是 。
② 图中方框内收集氨气的装置可选用 (填字母序号)。
③ 尾气处理装置中使用倒扣漏斗的作用是 。
(3)工业上用NH3制取NO反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.可用丁达尔现象区分溶液与胶体
B.生石灰与水混合的过程只发生物理变化
C.O3是由3个氧原子构成的化合物
D.CuSO4·5H2O是一种混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于实验的基本操作及安全知识的 叙述,正确的是
叙述,正确的是
A.蒸发食盐溶液时,发生液滴飞溅现象,立即加水冷却
B.实验室中将KMnO4与乙醇存放在同一橱柜中
C.配制硫酸溶液时,先在烧杯中加入一定体积的水,再在搅拌条件下慢慢加入浓硫酸
D.干燥SO2时,可以将其通过盛有浓硫酸的U形干 燥管
燥管
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸亚铁铵[(NH4)2SO4·FeSO4·6H2O]为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1 将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2 向处理过的铁屑中加入过量的3 mol·L-1H2SO4溶液,在60 ℃左右使其反应到不再产生气体,趁热过滤,得FeSO4溶液。
步骤3 向所得FeSO4溶液中加入饱和(NH4)2SO4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
(1)在步骤1的操作中,下列仪器中不必用到的有_______________________________
(填仪器编号);
①铁架台 ②燃烧匙 ③锥形瓶 ④广口瓶 ⑤研钵 ⑥玻璃棒 ⑦酒精灯
(2)在步骤2中所加的硫酸必须过量,其原因是________________________________
________________________________________________________________________。
(3)在步骤3中,“一系列操作”依次为____________________、________________和过滤。
(4)本实验制得的硫酸亚铁铵晶体常含有Fe3+杂质。检验Fe3+常用的试剂是____________,可以观察到的现象是_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验中,所采取的分离方法与对应原理都正确的是
| 选项 | 目的 | 分离方法 | 原理 |
| A | 分离溶于水的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |
| B | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
| C | 除去KNO3固体中混杂的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
| D | 除去丁醇中的乙醚 | 蒸馏 | 丁醇与乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
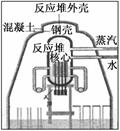 2013年3月11日,日本发生了9.0级地震并引发海啸,导致处于海边的福岛核电站发生系列爆炸。作为动力系统的核反应堆的第一层护罩是锆锡合金外壳,第二层护罩是压力仓(即一个坚固结实的大锅),第三层护罩用最坚固的钢和混凝土制成的非常厚的球体。下列叙述错误的是( )
2013年3月11日,日本发生了9.0级地震并引发海啸,导致处于海边的福岛核电站发生系列爆炸。作为动力系统的核反应堆的第一层护罩是锆锡合金外壳,第二层护罩是压力仓(即一个坚固结实的大锅),第三层护罩用最坚固的钢和混凝土制成的非常厚的球体。下列叙述错误的是( )
A.锆锡合金、钢、混凝土都属于混合物
B.钢的硬度和熔沸点都高于纯铁
C.锆锡合金和钢属于金属材料,混凝土属于传统的硅酸材料
D.在高温下,钢和水蒸气可发生反应产生氢气
查看答案和解析>>
科目:高中化学 来源: 题型:
磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重 要的应用。
要的应用。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)=6CaO(s)+P4(s)+10CO(g) △H1=+3359.26 kJ·mol-1
CaO(s)+SiO2(s)=CaSiO3(s) △H2=-89.61 kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)=6CaSiO3(s)+P4(s)+10CO(g) △H3
则△H3= kJ·mol-1。
(2)白磷中毒后可用CuSO4溶液解毒,解毒原理可用下列化学方程式表示:
11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4
60molCuSO4能氧化白磷的物质的量是 。
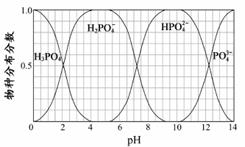
(3)磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH 的关系如右图所示。
①为获得尽可能纯的NaH2PO4,pH应控制在 ;pH=8时,溶液中主要含磷物种浓度大小关系为 。
②Na2HPO4溶液显碱性,若向溶液中加入足量的CaCl2溶液,溶液则显酸性,其原因是
(用离子方程式表示)。
(4)磷的化合物三氯氧磷( )与季戊四醇(
)与季戊四醇(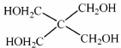 )以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X 的核磁共振氢谱如下图所示。
)以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X 的核磁共振氢谱如下图所示。
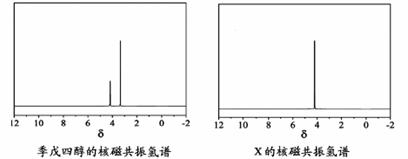
①酸性气体是 (填化学式)。
②X的结构简式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com