
【题目】食品检验是保证食品安全的重要措施,下列不属于食品安全检测指标的是( )
A. 淀粉的含量
B. 二氧化硫的含量
C. 亚硝酸盐的含量
D. 甲醛的含量
 灵星计算小达人系列答案
灵星计算小达人系列答案科目:高中化学 来源: 题型:
【题目】某烧碱样品中含有少量不与酸作用的可溶性杂质,为了测定其纯度,进行以下滴定操作:
A.在天平上准确称取烧碱样品wg,在烧坏中加蒸馏水溶解
B.在250mL容量瓶中定量成250mL烧碱溶液
C.用移液管移取25.00 mL烧碱溶液于锥形瓶中并滴加几滴甲基橙指示剂
D.将物质的量浓度为 Cmol/L 的标准盐酸 溶液装入酸式滴定管,调整液面,记下开始刻度数为Vml
E.在锥形瓶下垫一张白纸,滴定到终点,记录终点耗酸体积 V1ml
回答下列问题:
(1)操作中的雏形瓶下垫一张白纸的作用是__________________。
(2)操作中液面应调整到零刻度或零刻度以下(稍下)的某一刻度,尖嘴部分应___________。
(3)滴定终点时锥形瓶内溶液颜色变化是__________。
(4)若酸式滴定管没有用标准 润洗,会对测定结果有何影响_____________(填偏高、偏低或无影响,其他操作均正确)。
(5)该烧碱样品的纯度计算式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若X 最高正价与负价代数和为O,下列说法中不正确的是
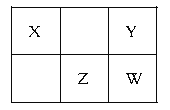
A. 元素X 形成化合物种类最多
B. 元素Y 可形成两种互为同素异形体的单质
C. 元素Z 最高价氧化物可干燥H2、O2等气体
D. 元素宰最高化合价为+7,且其单质具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.化学反应伴随能量变化,是化学反应的基本特征之一
B.常温下,氢氧化钡晶体与氯化铵晶体混合放出氨气,该反应为放热反应
C.化学反应中能量变化的大小与反应物的质量多少无关
D.旧化学键断裂所放出的能量高于新化学键形成所吸收的能量时发生放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
采用下图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为Na2SO3+SO2=Na2S2O5
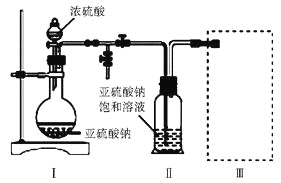
(1)装置Ⅰ中产生气体的化学方程式为____________________________。
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是____________。
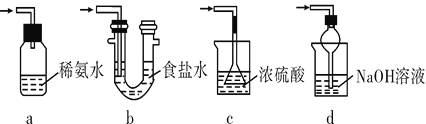
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为______(填字母)。
实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3。
(4)证明NaHSO3溶液中HSO![]() 的电离程度大于水解程度,可采用的实验方法是________(填字母)。
的电离程度大于水解程度,可采用的实验方法是________(填字母)。
a.测定溶液的pH
b.加入Ba(OH)2溶液
c.加入盐酸
d.加入品红溶液
e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验,是检验__________的存在(填离子符号)。
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:
(已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI)

①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为____________g·L-1。
②在上述实验过程中,若有部分HI被空气中氧化氧化,则测得结果________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH1,平衡常数为K1
FeO(s)+CO(g) ΔH1,平衡常数为K1
反应Fe(s)+H2O(g)![]() FeO(s)+H2(g) ΔH2,平衡常数为K2在不同温度时K1、K2的值如下表:
FeO(s)+H2(g) ΔH2,平衡常数为K2在不同温度时K1、K2的值如下表:
700 ℃ | 900 ℃ | |
K1 | 1.47 | 2.15 |
K2 | 2.38 | 1.67 |
反应CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH,平衡常数K,则ΔH=___________(用ΔH1和ΔH2表示),K=___________(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)
CO(g)+H2O(g) ΔH,平衡常数K,则ΔH=___________(用ΔH1和ΔH2表示),K=___________(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)![]() CO(g)+H2O(g)是________反应(填“吸热”或“放热”)。
CO(g)+H2O(g)是________反应(填“吸热”或“放热”)。
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)![]() FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示:
FeO(s)+CO(g) ΔH>0,CO2的浓度与时间的关系如图所示:
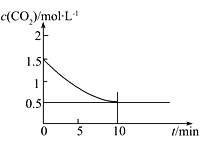
①该条件下反应的平衡常数为___________;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为____________mol·L-1。
②下列措施中能使平衡时![]() 增大的是__________(填序号) 。
增大的是__________(填序号) 。
A.升高温度 B.增大压强 C.再充入一定量的CO2 D.再加入一定量铁粉
③一定温度下,在一个固定容积的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是________(填字母)。
a. 容器中的压强不变 b.气体的密度不再改变
c. v正(CO2)=v逆(CO) d. c(CO2)=c(CO)
e. 容器内气体总物质的量不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁分别是氢氧化钙溶液、硝酸钾溶液、碳酸钠溶液、盐酸中的一种.已知甲和丙可以反应,甲和丁也可以反应,则下列说法正确的是( )
A. 甲一定是氢氧化钙溶液 B. 丁只能是盐酸
C. 丙不可能是碳酸钠溶液 D. 乙一定是硝酸钾溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对牙膏的探究要用到许多化学知识。
(1)下表列出了两种牙膏中的摩擦剂,请在表中填写两种摩擦剂所属的物质类别:
牙膏 | 珍珠王防臭牙膏 | 中华透明牙膏 |
摩擦剂 | 碳酸钙 | 二氧化硅 |
摩擦剂的物质类别(指酸、碱、盐、氧化物) |
(2)根据你的推测,牙膏摩擦剂的溶解性是__________(填“易溶”或“难溶”)。
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。甲同学设计了一种实验室制备碳酸钙的实验方案,其流程如下图所示:
![]()
请写出上述方案中有关反应的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________;
③________________________________________________________________________。
(4)乙同学的实验方案为:
![]()
其优点为____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com