
下列表示氯及其化合物的化学用语正确的是
A.中子数为20的氯原子符号:20Cl
B.HClO的结构式:H—Cl—O
C.HClO4的电离方程式:HClO4 H++ClO4-
H++ClO4-
D.Cl-的结构示意图:
科目:高中化学 来源:2016届山东省临沂市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列与化学概念有关的说法正确的是
A.SiO2、P2O5、NO均为酸性氧化物
B.NaH 、NaBH4 、NaClO均为离子化合物
C.NH3.H2O是弱碱,所以NH4NO3为弱电解质
D.磁性氧化铁、水玻璃、液氨均为混合物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高一上第二次月考化学试卷(解析版) 题型:实验题
铁做为重要的金属元素与人类生产生活密切相关,某课外活动小组在学习了氧化剂和还原剂后,要利用实验验证铁及其化合物的性质。
请你帮助他们完成以下实验报告:
(1)实验目的:探究铁及其化合物的氧化性和还原性
(2)试剂:铁粉、FeCl3溶液、FeCl2溶液、氯水、锌片、铜片
(3)仪器:胶头滴管, (你认为本实验必不可少的一种玻璃仪器)。
(4)实验记录(虚线部分不必填写)
序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为棕黄色 | Fe2+具有还原性 | |
② | 在FeCl2溶液中加入锌片 | Zn+Fe2+=Zn2++Fe | ||
③ | 在FeCl3溶液中加入足量铁粉 | Fe+2Fe3+=3Fe2+ | Fe3+具有氧化性 | |
④ | 溶液由黄色变为蓝色 | Fe3+具有氧化性 |
(5)实验结论:Fe只有还原性,Fe3+只有氧化性,Fe2+既有氧化性,又有还原性。
①根据以上结论判断,下列物质中既有氧化性,又有还原性的有: (填序号)。
A Cl2 B Na C Na+ D Cl- E NO2
②亚铁盐在溶液中易被氧化,而实验室中需要纯净的亚铁盐溶液。那么保存亚铁盐溶液时应该加入少量 防止亚铁盐被氧化。
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三上第四次月考化学试卷(解析版) 题型:选择题
下列晶体分类中正确的是一组是
离子晶体 | 原子晶体 | 分子晶体 | |
A | NaOH | Ar | SO2 |
B | H2SO4 | 石墨 | S |
C | CH3COONa | 水晶 |
|
D | Ba(OH)2 | 金刚石 | 玻璃 |
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三上四次模拟化学卷(解析版) 题型:填空题
X、Y、Z、W为四种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如下图所示:
X | Y | |
Z | W |
请回答下列问题:
(1)W位于周期表中第__________周期,第________族;
(2)X可形成双原子分子,其分子的电子式是___________;Y和氢元素形成的10电子微粒中常见的+1价阳离子为_________(填化学式,下同);Z和氢元素形成的18电子微粒中常见的-1价阴离子为__________;
(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式______________________。
(4)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡进有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式是_____________。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏银川二中高三上学期统考理综化学试卷(解析版) 题型:填空题
用含有Al2O3、SiO2和少量FeO·xFe2O3的铝灰制备Al2(SO4)3·18H2O,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量KMnO4溶液,调节溶液的pH约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色;
Ⅳ.加入MnSO4至紫红色消失,过滤;
Ⅴ..再经过一系列操作,分离得到产品。
(1)步骤Ⅰ中过滤所得滤渣主要成分为:______________________,H2SO4溶解Al2O3的离子方程式为:______________________。
(2)步骤Ⅱ中加入KMnO4时发生反应的离子方程式为:_______________________。
(3)已知:生成氢氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 3.4 | 6.3 | 1.5 |
完全沉淀时 | 4.7 | 8.3 | 2.8 |
注:金属离子的起始浓度均为0.1 mol·L-1
①根据表中数据解释步骤Ⅱ的目的:__________________________,
②当Al3+开始沉淀时,Fe3+的浓度约为:_______________________。
(4)已知:一定条件下,MnO4-可与Mn2+反应生成MnO2。
①向Ⅲ的沉淀中加入浓盐酸并加热,能说明沉淀中存在MnO2的现象是: 。
②步骤Ⅳ中加入MnSO4的目的是: 。
(5)步骤Ⅴ中“一系列操作”是________________________、________________________。
查看答案和解析>>
科目:高中化学 来源:2016届陕西省高三上12月模拟化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.尽管NO2能与水反应生成硝酸,但 NO2不属于酸性氧化物
B.Na2O 溶于水所得溶液能导电,据此可判断 Na2O属于电解质
C.氨气和氯化氢气体混合后生成的NH4Cl是离子化合物,因此该反应为离子反应
D.某气体只含N、H 两种元素,且质量之比为14︰3,则该气体一定为纯净物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省宜春市高一上学期第三次月考化学试卷(解析版) 题型:选择题
下列有关物质制备的反应中,其原理不属于氧化还原反应的是
A.工业制粗硅
B.湿法炼铜
C.用稀盐酸与石灰石反应制取CO2
D.稀硫酸与锌粒反应制取氢气
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二上学期第一次质检化学试卷(解析版) 题型:选择题
用惰性电极电解一定量的硫酸铜溶液,电解过程中的实验数据如图所示.横坐标表示转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).下列判断正确的是
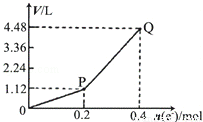
A.电解过程中,溶液的pH不断增大
B.Q点对应的气体中,H2与O2的体积比为2:1
C.阳极电极反应式为2H2O+4e﹣=4H++O2↑
D.当转移0.4mol e﹣时,电解生成的铜为6.4g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com