
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL溶液进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27g,经足量盐酸洗涤、千燥后,沉淀质量为2.33g。根据上述实验,以下推测正确的是( )
A.K一定存在B.100mL溶液中含0.01 mol CO32-
C.Cl-可能存在D.Ba2+一定不存在,Mg2+可能存在
【答案】AC
【解析】
①第一份加入AgNO3溶液有沉淀产生,与AgNO3溶液有沉淀产生的离子有:Cl-、CO32-、SO42-;
②加足量NaOH溶液加热产生0.04mol气体,该气体是氨气,故溶液中一定含有0.04mol NH4+;
③不溶于盐酸的2.33g沉淀为硫酸钡,物质的量为:![]() =0.01mol;6.27g沉淀是硫酸钡和碳酸钡,碳酸钡质量为6.27g-2.33g=3.94g,碳酸钡的物质的量为:
=0.01mol;6.27g沉淀是硫酸钡和碳酸钡,碳酸钡质量为6.27g-2.33g=3.94g,碳酸钡的物质的量为:![]() =0.02mol,故原溶液中一定存在CO32-、SO42-,则一定没有Mg2+、Ba2+,可能含有Cl-;
=0.02mol,故原溶液中一定存在CO32-、SO42-,则一定没有Mg2+、Ba2+,可能含有Cl-;
A.由分析可知,原溶液中n(SO42-)=0.01mol、n(CO32-)=0.02mol、n(NH4+)=0.04mol,由于溶液显电中性,2 n(SO42-)+2n(CO32-)=0.06mol> n(NH4+)=0.04mol,因此原溶液中,一定含有K+,且其物质的量n(K+)≥0.02mol,A符合题意;
B.由分析可知,原溶液中n(CO32-)=0.02mol,B不符合题意;
C.由分析可知,原溶液中可能含有Cl-,C符合题意;
D.由分析可知,原溶液中一定不含有Mg2+、Ba2+,D不符合题意;
故答案为:AC。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:
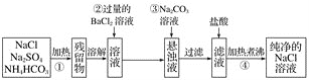
如果此方案正确,那么:
(1)操作①可选择_______仪器。
(2)操作②是否可改为加硝酸钡溶液__________,原因是___________。
(3)进行操作②后,判断硫酸根离子已除尽的方法是_____________。
(4)操作③的目的是_______,不先过滤后加碳酸钠溶液的理由是__________。
(5)操作④的目的是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某浓度的氨水中存在平衡:NH3·H2O![]() NH4++OH-,如想增大NH4+的浓度,而不增大OH-的浓度,应采取的措施是( )
NH4++OH-,如想增大NH4+的浓度,而不增大OH-的浓度,应采取的措施是( )
①适当升高温度 ②加入NH4Cl固体 ③通入NH3 ④加入少量盐酸
A.②④B.②③C.①②D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学依照如图所示流程提取海带中的碘元素。
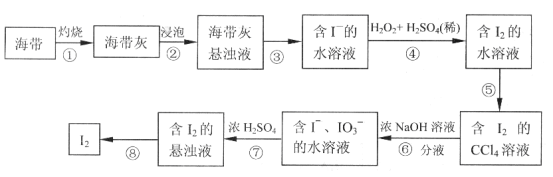
(1)步骤①中灼烧海带所用的仪器是___(填序号)。
a.试管 b.坩埚 c.烧杯 d.锥形瓶
(2)步骤④中用硫酸酸化的H2O2溶液将I-氧化成I2,反应的离子方程式是__。
(3)步骤⑤中采用的分离方法是___。
(4)经步骤⑤得到含I2的CCl4溶液后,继续采取步骤⑥⑦的目的是__。
(5)步骤⑦的反应中,当1molIO3-发生反应时,转移电子的物质的量是__mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列实验装置的说法正确的是( )
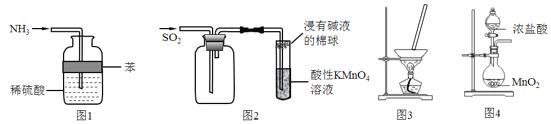
A.用图1吸收多余氨气且防止倒吸 B.用图2收集SO2并验证其还原性
C.图3蒸干NH4Cl饱和溶液制备NH4Cl晶体D.用图4实验室制取氯气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2O2是中学化学中一种重要的物质。请回答下列问题:
Ⅰ.一定条件下,烧杯中H2O2溶液发生分解反应放出气体的体积和时间的关系如图所示:

则由D到A过程中,随着反应的进行反应速率逐渐_________(选填 “加快”或“减慢”),其变化的原因是________________________________________。
Ⅱ.为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。
(1)定性图甲可通过观察_________定性比较得出结论。有同学提出将FeCl3溶液改为Fe2(SO4)3溶液更合理,其理由是_______。

(2)定量如图乙所示,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为_______,实验中需要测量的数据是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一小块金属钠,用滤纸吸干表面的煤油,用小刀切开后,可看到断面呈____色,具有_____光泽,但断面很快变___________,主要是由于生成一薄层_______。若把钠放在石棉网上加热,可观察到的现象是_______________ ,反应的化学方程式为_______其中还原剂为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为元素周期表的一部分:
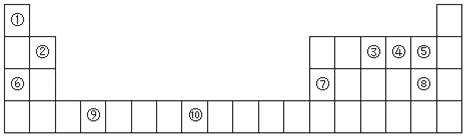
I.(1)元素③的基态原子轨道表示式为_________________。
(2)元素③④⑤的第一电离能由大到小的顺序为___________(填元素符号)。
(3)以下组合的原子间反应最容易形成离子键的是_____(选填A、B、C、D,下同)。
A.②和⑤ B.和⑤ C.⑤和⑥ D.⑥和⑧
(4)某些不同族元素的性质也有一定的相似性,如上表中元素⑦与元素②的单质及其化合物有相似的性质.写出元素②的最高价氧化物与NaOH溶液反应的离子方程式_________________________________。
II.(1)如图是部分元素原子的第一电离能I1随原子序数变化关系(其中12号至17号元素的有关数据缺失)。
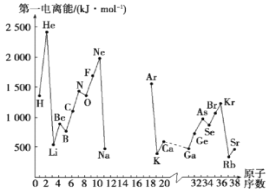
①根据同图示变化规律,可推测S的第一电离能的大小(最小)范围为___< S <___ (填元素符号)
②图中第一电离能最小的元素在周期表中的位置 ____________________
(2)用In表示元素的第n电离能,则图中的a、b、c分别代表(__________)
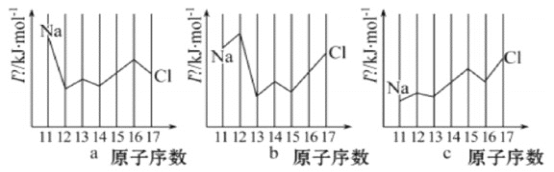
A.a为I1、b为I2、c为I3 B.a为I3、b为I2、c为I1
C.a为I2、b为I3、c为I1 D.a为I1、b为I3、c为I2
(3)铜、锌两种元素的第一电离能、第二电离能如表所示
电离能 | I1 | I2 |
Cu | 746 | 1958 |
Zn | 906 | 1733 |
铜的第一电离能(I1)小于锌的第一电离能,而铜的第二电离能(I2)却大于锌的第二电离能,其主要原因是______________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com