
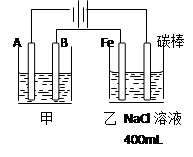
 ,②溶液变红。把湿润的碘化钾淀粉试纸放在碳棒附近,试纸变蓝色。(3)4.48L (4)1mol·L-1
,②溶液变红。把湿润的碘化钾淀粉试纸放在碳棒附近,试纸变蓝色。(3)4.48L (4)1mol·L-1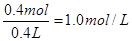


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
| A.CuSO4 | B.AgNO3 | C.KOH | D.H2SO4 E.NaCl F.Na2SO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.H2和Cl2 | B.Cu和Cl2 | C.H2和O2 | D.Cu和O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
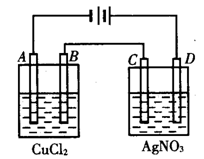
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cu(OH) 2 | B.Cu | C.CuSO4 | D.CuO |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
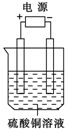
| | 电极材料 | 通电后的变化 | |
| 阴极 | 阳极 | ||
| A | 石墨 | 石墨 | 阴极质量增加,溶液的pH增大 |
| B | 铜 | 铜 | 阳极质量减小,阴极质量增加 |
| C | 铁 | 铁 | 两极的质量不发生变化 |
| D | 铂 | 铁 | 阴极质量增加,溶液的浓度不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com