
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
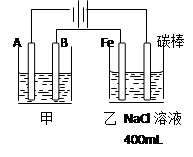
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
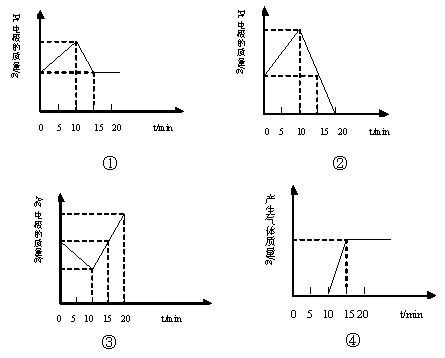
| A.①③ | B.①②③ | C.②③④ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
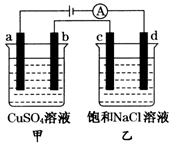
A.乙池中d的电极反应为 |
| B.a,c两极产生气体的物质的量相等 |
| C.甲、乙两池中溶液pH均保持不变 |
D.乙池中发生的反应为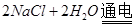 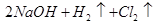 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1∶8 | B.8∶1 | C.35.5∶108 | D.108∶35.5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 ,下列说法正确的是
,下列说法正确的是| A.放电时正极反应为:VO+2+2H++e—=VO2+ +H2O |
| B.放电时每转移2mol电子时,消耗1mol氧化剂 |
| C.放电过程中电子由负极经外电路移向正极,再由正极经电解质溶液移向负极 |
| D.放电过程中,H+由正极移向负极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.AgNO3 | B.H2SO4? | C.NaOH | D.NaCl? |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 在工业生产和日常生活中有重要用途。 I.工业上用钛矿石(
在工业生产和日常生活中有重要用途。 I.工业上用钛矿石( ,含
,含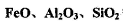 等杂质)经过下述反应制得:
等杂质)经过下述反应制得:
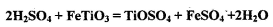
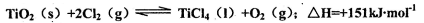
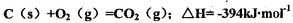
 与Cl2、C反应制取TiO4的热化学方程式:____________
与Cl2、C反应制取TiO4的热化学方程式:____________查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
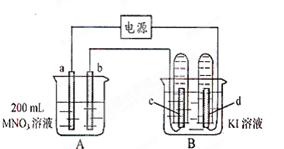

 。电解进行一段时
。电解进行一段时 也收集到了气体,此时c极上的电极反应式为: 。
也收集到了气体,此时c极上的电极反应式为: 。 溶液的物质的量浓度为 mol·L-1。
溶液的物质的量浓度为 mol·L-1。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com