
| A. | 向pH=4的溶液中滴加BaCl2溶液,会有白色沉淀产生 | |
| B. | pH=4.5时c(H2SO3)+c(H+)=c(SO32-)+c(OH-) | |
| C. | pH=5时c(Na+)>c(HSO3-)>c(SO32-)>c(H+)>c(OH-) | |
| D. | 向pH=5.5的溶液中滴加溴水,反应的离子方程式为H2SO3+Br2+H2O=4H++SO42-+2Br- |
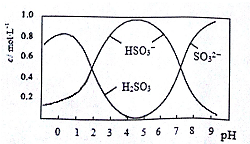
分析 A.pH=4的溶液中主要是HSO3-和少量H2SO3,加入BaCl2溶液无沉淀生成;
B.根据图可知,pH=4.5时,溶液中主要以亚硫酸氢根离子形式存在,溶液中存在电荷守恒和物料守恒分析判断;
C.pH=5时主要是HSO3-和少量SO32-溶液显酸性;
D.pH=5.5的溶液中主要是HSO3-和少量SO32-溶液显酸性,无H2SO3;
解答 解:A.pH=4的溶液中主要是HSO3-和少量H2SO3,溶液中亚硫酸根离子不能结婚钡离子生成沉淀,加入BaCl2溶液无沉淀生成,故A错误;
B.pH=4.5时,溶液中主要以亚硫酸氢根离子形式存在,溶液中存在电荷守恒和物料守恒,c(Na+)+c(H+)=2c(SO32-)+c(OH-)+c(HSO3-),c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3),得到c(H2SO3)+c(H+)=c(SO32-)+c(OH-),故B正确;
C.pH=5时主要是HSO3-和少量SO32-溶液显酸性,c(SO32-)<c(H+),故C错误;
D.pH=5.5的溶液中主要是HSO3-和少量SO32-溶液显酸性,无H2SO3 向pH=5.5的溶液中滴加溴水反应是HSO3-被溴单质氧化,故D错误;
故选B.
点评 本题考查了电解质溶液中离子浓度大小比较、电荷守恒和物料守恒、主要是图象变化分析和离子存在的判断,掌握基础是解题关键,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 最高正价为+3价 | B. | 其最低负价可能为-1价 | ||
| C. | 氢化物易溶于水 | D. | 是活泼的非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
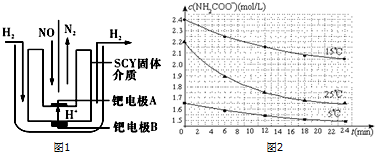
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度(×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 是一种高效麻醉剂,该有机物同分异构体中含有羧基和氨基,且苯环上有2个取代基的有(不考虑立体异构)( )
是一种高效麻醉剂,该有机物同分异构体中含有羧基和氨基,且苯环上有2个取代基的有(不考虑立体异构)( )| A. | 18种 | B. | 15种 | C. | 13种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
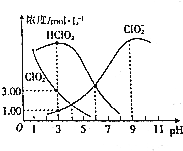 亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,在水溶液中可生成Cl02、HClO2、ClO2-、Cl-等,经测定,25℃时某浓度的NaClO2溶液中各组分含量随pH变化情况如图所示(Na+、Cl-没有画出).下列有关该溶液的说法不正确的是( )
亚氯酸钠(NaClO2)是一种高效氧化剂、漂白剂,在水溶液中可生成Cl02、HClO2、ClO2-、Cl-等,经测定,25℃时某浓度的NaClO2溶液中各组分含量随pH变化情况如图所示(Na+、Cl-没有画出).下列有关该溶液的说法不正确的是( )| A. | 亚氯酸钠在碱性条件下较稳定 | |
| B. | HClO2的电离平衡常数Ka=10-6 | |
| C. | pH=3时,c(Cl-)>c(ClO2-) | |
| D. | pH=4时,c(Cl-)+c(ClO2-)-c(Na+)=10-4-10-10 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{94}^{238}$Pu与${\;}_{92}^{238}$U互为同位素 | |
| B. | ${\;}_{94}^{238}$Pu与${\;}_{94}^{239}$Pu具有相同的最外层电子数 | |
| C. | ${\;}_{94}^{238}$Pu与${\;}_{94}^{239}$Pu具有相同的中子数 | |
| D. | ${\;}_{94}^{238}$Pu与${\;}_{92}^{238}$U具有完全相同的化学性质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com