
【题目】下列物质中属于电解质的是( )
A.酒精
B.氨水
C.氯化钠
D.二氧化碳
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中存在下列平衡:CO(g)+H2O(g)![]() CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
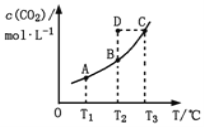
A. 反应CO(g)+H2O(g)![]() CO2(g)+H2(g)的 ΔH>0
CO2(g)+H2(g)的 ΔH>0
B. 在T2时,若反应处于状态D,则一定有ν正<ν逆
C. 平衡状态A与C相比,平衡状态A的c(CO)小
D. 若T1、T2时的平衡常数分别为K1、K2,则K1<K2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)火箭的第一、二级发动机中,所用的燃料为偏二甲肼和四氧化二氮,偏二甲肼可用肼来制备。
①用肼(N2H4)作燃料,四氧化二氮作氧化剂,两者反应生成氮气和气态水。
已知:N2(g)+2O2(g)===N2O4(g)
ΔH=+10.7 kJ·mol-1
N2H4(g)+O2(g)===N2(g)+2H2O(g)
ΔH=-543 kJ·mol-1
写出气态肼和N2O4反应的热化学方程式: ___________________。
②已知四氧化二氮在大气中或在较高温度下很难稳定存在,它很容易转化为二氧化氮。试推断出二氧化氮制取四氧化二氮的反应条件(或措施):___________________________。
(2)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航空航天。如图1所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-离子(O2+4e-===2O2-)。

①c电极的名称为________,d电极上的电极反应式为_________________________。
②如图2所示为电解100 mL 0.5 mol·L-1CuSO4溶液,a电极上的电极反应式为____________________。若a电极产生56 mL(标准状况)气体,则所得溶液的pH=________(不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入________(填序号)。
a.CuO b.Cu(OH)2
c.CuCO3 d.Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A. HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热也是△H=-57.3kJ/mol
B. CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g) △H=+566kJ/mol
C. 需要加热才能发生的反应一定是吸热反应
D. 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃煤烟气脱硫有很多方法
方法I:先用氨水将SO2转化为NH4HSO3,再通入空气氧化成(NH4)2SO4。
方法II:用Na2SO3溶液吸收S02,再经电解转化为H2SO4。
据此回答以下问题:
(1)方法I中发生氧化还原反应的离子方程式__________。能提高方法I燃煤烟气SO2中去除率的措施有__________(填字母)。
A.增大氨水浓度 B.增大燃煤烟气的流速
C.事先去除燃煤烟气中的二氧化碳 D.增大压强
(2)采用方法II脱硫,燃煤烟气中的二氧化碳能否与生成的NaHSO3溶液反应_______(说明理由)。已知H2SO3为的电离平衡常数为K1=1.54×10-2,K2=1.02×10-7。则NaHSO3溶液中含S元素粒子浓度由大到小的顺序为_______。通过右图所示电解装置可将生成的NaHSO3转化为硫酸,电极材料皆为石墨。则A为电解池的______(填“阴极”或“阳极”)。C为______(填物质名称)。若将阴离子交换膜换成阳子交换膜,写出阳极区域发生的电极反应______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式错误的是 ( )
A.NaHCO3 = Na++H++CO32- B.NaHSO4 = Na++H++SO42-
C.Mg(NO3)2 = Mg2++2NO3- D.Na2SO4 = 2Na++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中气体作氧化剂的是( )
A.SO3通入水中:SO3+H2O═H2SO4
B.Cl2通入FeCl2溶液中:Cl2+2FeCl2═2FeCl3
C.HCl气体通入NaOH溶液中:HCl+NaOH═NaCl+H2O
D.CO2通入NaOH溶液中:CO2+2NaOH═Na2CO3+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com