
(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6 kJ的热量,试写出对应的热化学方程式 。标准状况下11.2L氢气在氯气中充分燃烧放出的热量是 kJ。
(2)A(g)+B(g) C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
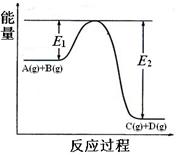
①反应物A(g)和B(g)具有的总能量 (填大于、小于、等于)生成物C(g)和D(g)具有的总能量。
②该反应是_______反应(填吸热、放热),△H= (用E1和E2表示)。
③稳定性:反应物 生成物(填大于、小于、等于)。
(1) H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ?mol-1 。 92.3 kJ。
(2)① 大于 ;②放热,△H=E1-E2 ③ 小于
【解析】
试题分析:(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6 kJ的热量,则该反应的热化学方程式是H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ/mol。标准状况下11.2L氢气的物质的量是0.5mol,在氯气中充分燃烧放出的热量是184.6 kJ/mol×0.5mol=92.3kJ。
(2)①根据图像可知,反应物的总能量高于生成物的总能量,所以反应是放热反应。则反应物A(g)和B(g)具有的总能量大于生成物C(g)和D(g)具有的总能量。
②该反应是反应放热反应,△H=E1-E2。
③反应物的总能量高,所以稳定性是反应物小于生成物的。
考点:考查反应热的计算以及热化学方程式书写
点评:该题是中等难度试题的考查,主要是考查学生对热化学方程式书写以及反应热计算的熟悉了解程度,旨在巩固学生的基础,提高学生的应试能力,有利于调动学生的学习兴趣和学习积极性。


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
![]()
化合物A经下列四步反应可得到常用溶剂四氢呋喃,反应框图如下:
请完成下列问题:
(1)1molA和1mol氢气在一定条件下恰好反应,生成饱和一元醇Y,Y中碳元素的质量分数约为65%,则Y的分子式为:__________________。
(2)第①②步反应类型分别为:_________________,________________。
(3)化合物B具有的化学性质(填写字母代号)是:_________。
a.可发生氧化反应 b.强酸或强碱条件下均可发生消去反应
c.可发生酯化反应 d.催化条件下可发生加聚反应
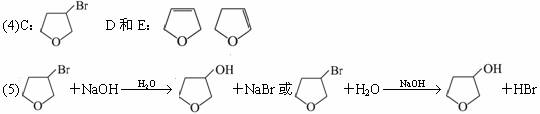
(4)写出C、D、E的结构简式:
C:_____________,D:_____________,E:________________。
(5)写出化合物C与氢氧化钠水溶液反应的化学方程式:
_______________________________________________________。
(6)写出四氢呋喃链状的所有同分异构体的结构简式:_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(本题有3小题)(共10分)
I.(2分)下列两个图示,A所表示的是--------------热反应,B所表示的是--------------热反应。
A B
II.(2分)在氢气与氯气反应生成氯化氢气体的反应中,若断裂1mol H - H键要吸收436KJ的能量,断裂1mol Cl- Cl键要吸收243KJ的能量,断裂1molH - Cl键要吸收432KJ的能量,则表示1mol 氢气在氯气中充分燃烧的热化学方程式是 。
III.(5分)如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入5ml盐酸于试管中,试回答下列问题:

(1)实验中观察到的现象是试管中 ,烧杯中析出晶体。
(2)写出试管中反应的离子反应方程式 ,
(3)由此推知,MgCl2溶液和H2的总能量 填(“大于”“小 于”或“等于”)镁片和盐酸的总能量
查看答案和解析>>
科目:高中化学 来源:2012-2013学年浙江宁波万里国际学校高一下学期期中考试化学试卷(带解析) 题型:填空题
(1)1mol氢气在氯气中充分燃烧生成氯化氢气体时放出184.6 kJ的热量,试写出对应的热化学方程式 。标准状况下11.2L氢气在氯气中充分燃烧放出的热量是 kJ。
(2)A(g)+B(g) C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量(kJ)变化如图所示,回答下列问题。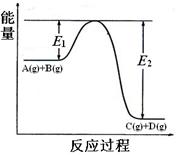
①反应物A(g)和B(g)具有的总能量 (填大于、小于、等于)生成物C(g)和D(g)具有的总能量。
②该反应是_______反应(填吸热、放热),△H= (用E1和E2表示)。
③稳定性:反应物 生成物(填大于、小于、等于)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com