
| A.向氯化铝溶液中滴加过量氨水,反应的离子方程式是:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B.足量铜与含1 mol溶质的浓硫酸反应,可生成0.5 mol SO2 |
| C.碱性锌锰电池工作时,电子由MnO2经外电路流向Zn 极 |
| D.15.6 g过氧化钠与足量二氧化碳充分反应,转移电子数为1.204×1023 |
| 15.6g |
| 78g/mol |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2的燃烧热△H=-241.8kJ?mol-1 | B、炭和和水蒸气转化为水煤气为放热反应 | C、将24g 炭完全转化为水煤气,再充分燃烧,整个过程反应热为-787.0kJ?mol-1 | D、1mol H2O(g)完全分解需要吸收241.8kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
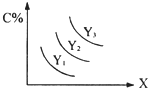 对于反应A(s)+2B(g?3C(g);△H>0,C%跟外界条件X、Y的关系如图所示,下列结论正确的是( )
对于反应A(s)+2B(g?3C(g);△H>0,C%跟外界条件X、Y的关系如图所示,下列结论正确的是( )| A、Y表示温度,X表示压强,且Y3>Y2>Y1 | B、Y表示压强,X表示温度,且Y3>Y2>Y1 | C、X表示压强,Y表示温度,且Y1>Y2>Y3 | D、X表示温度,Y表示压强,且Y1>Y2>Y3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com