
【题目】现有金属A、B和气体甲、乙、丙及物质C、D、F、F,它们之间的转化发生如下反应,(图中有些反应的产物和反应条件没有全部标出),其中B是地壳中含量最高的金属元素,反应④在野外经常用来焊接铁轨.
请回答下列问题:
(1)写出金属A与水反应的离子方程式 .
(2)写出反应④化学方程式: .
(3)气体甲在黄绿色气体乙中燃烧的现象: .
(4)金属单质A投入到下列溶液中既有气体,又有沉淀出现的是
A.氯化钠溶液
B.碳酸钠溶液
C.硫酸铜溶液
D.氯化铵溶液.
【答案】
(1)2Na+2H2O=2Na++2OH﹣+H2↑
(2)2Al+Fe2O3 ![]() Al2O3+2Fe
Al2O3+2Fe
(3)燃烧,发出苍白色火焰,瓶口出现白雾
(4)C
【解析】解:金属A焰色反应为黄色证明为Na,与水反应生成气体甲为H2 , 物质C为NaOH,B是地壳中含量居第一的金属元素为Al,黄绿色气体乙为Cl2 , 氢气与氯气反应得气体丙为HCl,溶于水得到溶液D为盐酸溶液,盐酸与铝反应生成物质E为氯化铝,反应④在野外经常用来焊接铁轨,应为铝热反应,即氧化铁与铝高温条件下反应生成铁和氧化铝,(1)钠与水反应的离子方程式为2Na+2H2O=2 Na++2OH﹣+H2↑,所以答案是:2Na+2H2O=2 Na++2OH﹣+H2↑;(2)反应④为铝热反应,即氧化铁与铝高温条件下反应生成铁和氧化铝,反应方程式为2Al+Fe2O3 ![]() Al2O3+2Fe,所以答案是:2Al+Fe2O3
Al2O3+2Fe,所以答案是:2Al+Fe2O3 ![]() Al2O3+2Fe;(3)甲为H2 , 甲在黄绿色气体乙中燃烧的现象为燃烧,发出苍白色火焰,瓶口出现白雾,所以答案是:燃烧,发出苍白色火焰,瓶口出现白雾;(4)A、钠投入氯化钠溶液中,钠与水反应有气体产生,无沉淀;B、钠投入碳酸钠溶液中,钠与水反应有气体产生,无沉淀;C、钠投入硫酸铜溶液中,钠与水反应有气体产生,同时产生氢氧化钠,氢氧化钠与硫酸铜反应产生氢氧化铜沉淀;D、钠投入氯化铵溶液中,钠与水反应有气体产生,同时产生氢氧化钠,氢氧化钠与氯化铵溶液反应产生氨气,无沉淀;故选C.
Al2O3+2Fe;(3)甲为H2 , 甲在黄绿色气体乙中燃烧的现象为燃烧,发出苍白色火焰,瓶口出现白雾,所以答案是:燃烧,发出苍白色火焰,瓶口出现白雾;(4)A、钠投入氯化钠溶液中,钠与水反应有气体产生,无沉淀;B、钠投入碳酸钠溶液中,钠与水反应有气体产生,无沉淀;C、钠投入硫酸铜溶液中,钠与水反应有气体产生,同时产生氢氧化钠,氢氧化钠与硫酸铜反应产生氢氧化铜沉淀;D、钠投入氯化铵溶液中,钠与水反应有气体产生,同时产生氢氧化钠,氢氧化钠与氯化铵溶液反应产生氨气,无沉淀;故选C.


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】下列物质在给定条件下同分异构体数目正确的是( )
A.C4H10属于烷烃的同分异构体有3种
B.结构为 ![]() 的一溴代物有5种
的一溴代物有5种
C.分子组成是C4H8O属于醛类的同分异构体有3种
D.分子组成是C5H10O2属于羧酸的同分异构体有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是()
A. 打开汽水瓶有气泡从溶液中冒出
B. 实验室用排饱和食盐水法收集氯气
C. 合成氨工厂采用增大压强以提高原料的转化率
D. 2NO2(g)![]() N2O4(g)的平衡体系中, 加压缩小体积后颜色加深
N2O4(g)的平衡体系中, 加压缩小体积后颜色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)是一种一元中强酸,具有较强的还原性.试回答下列问题:
(1)P的原子结构示意图为;
(2)NaH2PO2为(填“正盐”或“酸式盐”),溶液中有关离子浓度从大到小的顺序为 .
(3)H3PO2可将溶液中的银离子还原为银单质,若氧化剂与还原剂的物质的量之比为4:1,则该反应的氧化产物的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、生产密切相关,下列有关说法错误的是( )
A. 高纯单质硅用于制光电池B. 酸雨是指pH<5.6的雨水
C. 二氧化硫可大量用于食品增白D. 常温下,铁制容器可用于存贮浓硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】雾霾含有大量的污染物SO2、NO.工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如图1(Ce为铈元素):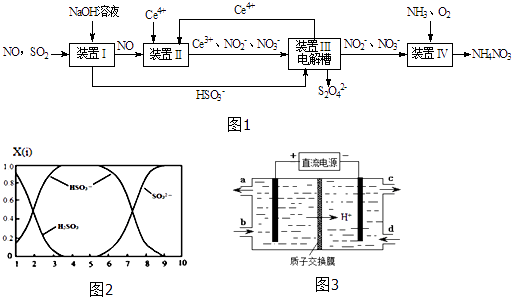
(1)装置Ⅰ中的主要离子方程式为 .
(2)含硫各微粒(H2SO3、HSO3﹣和SO32﹣)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图2所示.①若是0.1mol NaOH反应后的溶液,测得溶液的pH=8时,溶液中个离子由大到小的顺序是 .
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因: .
(3)写出装置Ⅱ中,酸性条件下的离子方程式 .
(4)装置Ⅲ还可以使Ce4+再生,其原理如图3所示.①生成Ce4+从电解槽的(填字母序号)口流出.
②写出与阴极的反应式 .
(5)已知进入装置Ⅳ的溶液中,NO2﹣的浓度为a gL﹣1 , 要使1m3该溶液中的NO2﹣完全转化为NH4NO3 , 需至少向装置Ⅳ中通入标准状况下的O2L.(用含a代数式表示,计算结果保留整数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】滴定实验是化学学科中重要的定量实验.请回答下列问题:
Ⅰ.酸碱中和滴定﹣﹣已知某NaOH试样中含有NaCl杂质,为测定试样中NaOH的质量分数,进行如下步骤实验:
①称量1.00g样品溶于水,配成250mL溶液; ②准确量取25.00mL所配溶液于锥形瓶中;③滴加几滴酚酞溶液;④用0.10mol/L的标准盐酸滴定三次,每次消耗盐酸的体积记录如下:
滴定序号 | 待测液体积 | 所消耗盐酸标准的体积(mL) | |
滴定前 | 滴定后 | ||
1 | 25.00 | 0.50 | 20.60 |
2 | 25.00 | 6.00 | 26.00 |
3 | 25.00 | 1.10 | 21.00 |
(1)用滴定管(填“酸式”或“碱式”)盛装0.10mol/L的盐酸标准液.
(2)试样中NaOH的质量分数为 .
(3)若出现下列情况,测定结果偏高的是 .
a.滴定前用蒸馏水冲洗锥形瓶
b.在振荡锥形瓶时不慎将瓶内溶液溅出
c.若在滴定过程中不慎将数滴酸液滴在锥形瓶外
d.酸式滴定管滴至终点对,俯视读数
e.酸式滴定管用蒸馏水洗后,未用标准液润洗
(4)Ⅱ.氧化还原滴定﹣取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1molL﹣1的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+10CO2↑+2MnSO4+8H2O.滴定时,KMnO4溶液应装在酸式滴定管中,滴定终点时滴定现象是
(5)Ⅲ.沉淀滴定﹣﹣滴定剂和被滴定物的生成物比滴定剂与指示剂的生成物更难溶.参考下表中的数据,若用AgNO3滴定NaSCN溶液,可选用的指示剂是 (填选项字母).
难溶物 | AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN |
颜色 | 白 | 浅黄 | 白 | 砖红 | 白 |
Ksp | 1.77×10﹣10 | 5.35×10﹣13 | 1.21×10﹣16 | 1.12×10﹣12 | 1.0×10﹣12 |
A.NaCl
B.NaBr
C.NaCN
D.Na2CrO4 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇的沸点比含相同碳原子的烷烃的沸点高的主要原因是( )
A.乙醇的分子量比含相同碳原子的烷烃的分子量大
B.乙醇分子之间易形成氢键
C.碳原子与氢原子的结合程度没碳原子与氧原子的结合程度大
D.乙醇是液体,而乙烷是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一个化学过程的示意图. 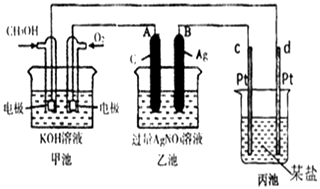
(1)请回答图中甲池是装置,其中OH﹣移向极(填“正”或“负”)
(2)写出通入CH3OH的电极反应式是
(3)向乙池两电极附近滴加适量紫色石蕊试液,附近变红的电极为极(填“A”或“B”),并写出此电极反应的电极反应式 .
(4)乙池中反应的离子方程式为 .
(5)当乙池中B(Ag)极的质量增加2.70g时,乙池的pH是(若此时乙池中溶液的体积为250mL);此时丙池某电极析出0.80g某金属,则丙中的某盐溶液可能是(填序号)
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com