
| 化学式 | CH3COOH | HClO | H2CO3 |
| Ka | 1.8×10-5 | 3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
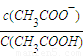 =4.8+lg
=4.8+lg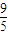 =5.055≈5,故B正确;
=5.055≈5,故B正确;

 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:2013年山东省德州市高考化学一模试卷(解析版) 题型:解答题
| T/(K) | 298 | 398 | 498 | … |
| K/-2 | 4.1×106 | K1 | K2 | … |
 ]>[NH
]>[NH ]>[H+]>[OH-]
]>[H+]>[OH-] ]>[SO
]>[SO ]>[OH-]>[H+]
]>[OH-]>[H+] ]+[H+]>[SO
]+[H+]>[SO ]+[OH-]
]+[OH-]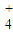 ]>[SO
]>[SO ]>[H+]>[OH-].
]>[H+]>[OH-].查看答案和解析>>
科目:高中化学 来源:2013年安徽省淮南市高考化学一模试卷(解析版) 题型:解答题
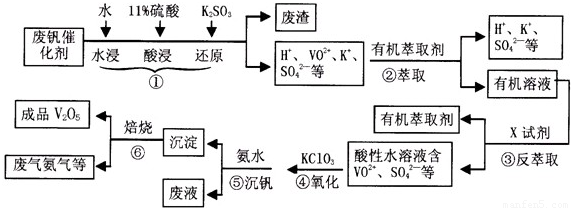
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
查看答案和解析>>
科目:高中化学 来源:2013年山东省淄博市高考化学一模试卷(解析版) 题型:解答题
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | AlOH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
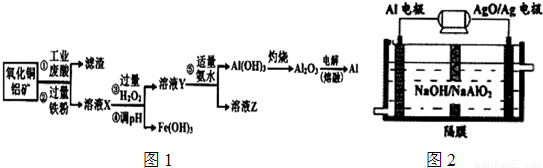
查看答案和解析>>
科目:高中化学 来源:2012年浙江省高考化学模拟试卷(解析版) 题型:选择题
| 化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
| Ksp或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com