
【题目】下列说法不正确的是
A. 碘化银可用于人工降雨 B. 海水中含量最高的非金属元素是氯元素
C. 晶体硅常用于制造集成电路 D. 氧化镁可做耐高温材料
 优生乐园系列答案
优生乐园系列答案科目:高中化学 来源: 题型:
【题目】在铜与浓硫酸的反应中,如果转移0.4mol电子,则被还原的硫酸物质的量
A. 0.4mol B. 0.2mol
C. 小于0.4mol D. 小于0.2 mol
【答案】B
【解析】
铜与浓硫酸的反应中,铜元素化合价升高,失去电子,硫元素化合价降低,得到电子,得失电子总数是相等的,均为0.4mol。
Cu和浓硫酸反应方程式为Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,由方程式可知,1mol硫酸被还原时转移电子物质的量=1mol×(6-4)=2mol,所以如果电子转移0.4mol,则被还原的硫酸的物质的量0.2mol,答案选B。
CuSO4+SO2↑+2H2O,由方程式可知,1mol硫酸被还原时转移电子物质的量=1mol×(6-4)=2mol,所以如果电子转移0.4mol,则被还原的硫酸的物质的量0.2mol,答案选B。
【点睛】
本题考查氧化还原反应的计算,侧重考查分析计算能力,知道作氧化剂的浓硫酸和转移电子的关系,明确浓硫酸的作用是解本题关键。
【题型】单选题
【结束】
18
【题目】下列离子方程式书写正确的是
A. 向Fe(OH)3中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
B. NH4HSO3溶液与足量的NaOH溶液混合加热:NH4++HSO3-+2OH-![]() NH3↑+SO32-+2H2O
NH3↑+SO32-+2H2O
C. 酸性条件下KIO3溶液与KI溶液发生反应生成I2:IO3-+5I-+3H2O=3I2+6OH-
D. 向FeO中加入稀硫酸:2FeO + 8H+ + SO42- =2Fe3+ + SO2 ↑+ 4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t ℃时,0.01 mol/L NaOH溶液pH=11,0.1 mol/LHA溶液中![]() =109。
=109。
(1)该温度下,水的离子积Kw=________,HA是________(填“强”或“弱”)酸。
(2)该温度下,将pH之和为13的NaOH溶液和HA溶液等体积混合后,所得溶液呈_____(填“酸”、“碱”或“中”)性,理由是____________________________________。
(3)在室温下,用蒸馏水稀释0.01 mol/L HA溶液时,下列呈减小趋势的是________。
A.![]() B.
B.![]() C.溶液中c(H+)和c(OH-)的乘积
C.溶液中c(H+)和c(OH-)的乘积
D.溶液中c(A-)·c(HA)的值 E.水的电离程度
(4)室温下,取pH=2的盐酸和HA溶液各100 mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如下图所示:

①图中表示HA溶液pH变化曲线的是________(填“A”或“B”)。
②设盐酸中加入Zn的质量为m1,HA溶液中加入Zn的质量为m2,则m1________m2(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在某密闭容器中进行如下反应:
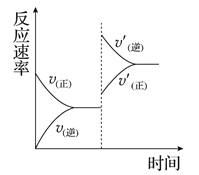
mA(g)+nB(g)![]() pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,
pC(g)+qD(g),若增大压强或升高温度,重新达到平衡,
反应速率随时间的变化过程如图所示,则对该反应的叙述正确的是( )
A. 正反应是吸热反应 B. 逆反应是放热反应
C. m+n<p+q D. m+n>p+q
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海带中提取碘有如下步骤:①通入足量的Cl2,②将海带焙烧成灰后加水搅拌,③加CCl4振荡,④用分液漏斗分液,⑤过滤。合理的操作顺序是( )
A.①②③④⑤B.②⑤①③④C.①③⑤②④D.②①③⑤④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示细胞内某些有机物的元素组成和功能关系,其中A、B代表元素,Ⅰ、Ⅱ、Ⅲ、Ⅳ是生物大分子,图中X、Y、Z、P分别为构成生物大分子的基本单位.请回答下列问题:
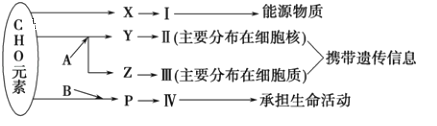
(1)图中X是_____,Ⅰ在小麦种子中主要是指_____。
(2)图中Z是_____,使用甲基绿、吡罗红混合染液染色,可使Ⅲ呈现_____色。
(3)图中P的结构通式为___________;写出由P形成Ⅳ的结构层次依次为________________________。
(4)鉴定Ⅳ时需使用双缩脲试剂,应先加_____,造成碱性环境,再加_____。(填试剂名称)
(5)分析如图中化合物的结构,回答问题。

该化合物中④表示_______。该化合物是由_____种氨基酸通过脱水缩合方式形成的,该化合物叫____________,若完全水解成为氨基酸则需要_______个水分子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用能量判断下列过程的方向的是
A、水总是自发地由高处往低处流
B、有序排列的火柴散落时成为无序排列
C、放热反应容易进行,吸热反应不能自发进行
D、多次洗牌以后,扑克牌的毫无规律的混乱排列的几大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)①相同质量的SO2、SO3的物质的量之比为________;
②氧原子的个数之比为________。
(2)12.4 g Na2R含Na+0.4 mol,则Na2R的摩尔质量为________,R的相对原子质量为________。含R的质量为1.6 g的Na2R,其物质的量为________。
(3)相同条件下10mLA2气体与30mLB2气体恰好完全反应生成20mL某气体C,则C的化学式为__________________(用A、B表示),推断中用到的原理理论是:______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com