
【题目】过氧化钙是一种白色固体,常用作杀菌剂、防腐剂。
(1)化学实验小组选用如下装置(部分固定装置略)用钙和氧气制备过氧化钙。

①请选择必要的装置(装置可重复使用),按气流方向连接顺序为__________________。(填仪器接口的字母编号)
②连接好装置进行实验,步骤如下:
I.检查装置气密性后,装入药品;
II._____________________;
III.点燃B处酒精灯加热药品;反应结束后,_______________________________;
Ⅳ.拆除装置,取出产物。
(2)已知化学反应Ca2++H2O2+2NH3+8H2O= CaO2·8H2O↓+2NH4+。在碱性环境中制取CaO2·8H2O的装置如下图:
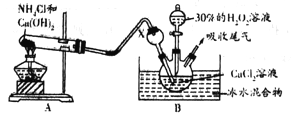
①装置B中仪器X的作用是__________________________________;反应在冰水浴中进行的原因是__________________________________________________________。
②反应结束后,经________、__________、低温烘干获得CaO2·8H2O。
【答案】 a e d b c e 打开分液漏斗活塞,通一段时间气体 先熄灭酒精灯,待产品冷却后再停止通入氧气 导气,防止倒吸 防止温度过高H2O2分解;有利于晶体析出 过滤 洗涤
【解析】本题考查过氧化钙的制备、性质及化学实验操作的知识。(1) ①用双氧水与二氧化锰反应产生氧气,用浓硫酸干燥氧气,氧气与Ca在加热时发生反应产生过氧化钙,为了防止空气中的水分影响反应产物,应该再通过盛有浓硫酸的洗气瓶。故装置的连接顺序是a→e→d→b→c→e;②连接好装置进行实验,步骤如下:I.检查装置气密性后,装入药品;II. 打开分液漏斗活塞,通一段时间气体,排除装置中的气体;III.点燃B处酒精灯加热药品;反应结束后,先熄灭酒精灯,待产品冷却后再停止通入氧气,防止发生倒吸;Ⅳ.拆除装置,取出产物;(2)①氨气极易溶于水,故装置B中仪器X的作用是导气,防止倒吸;因双氧水易分解,故在冰水浴中进行的原因是防止温度过高H2O2分解;有利于晶体析出;②反应结束后,将B装置中三颈烧瓶中的物质进行过滤、洗涤、低温烘干获得CaO2·8H2O。


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.具有规则几何外形的固体一定是晶体
B.晶体与非晶体的根本区别在于是否具有规则的几何外形
C.具有各向异性的固体一定是晶体
D.晶体、非晶体都具有固定的熔点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于实验的说法正确的是( )
A. 制备溴苯时可以用苯和溴水反应
B. 制备溴苯的装置中,长直玻璃导管主要起导气和冷凝回流的作用
C. 苯的硝化反应可用酒精灯直接加热
D. 制硝基苯过程中浓硫酸的作用是脱水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将NaHCO3溶液跟Al2(SO4)3溶液混合,相关反应的离子方程式是____________。
(2)有浓度均为0.2 mol·L-1的Na2CO3溶液与NaHCO3溶液,试回答下列问题:
①微粒种类:Na2CO3__________NaHCO3溶液(填“﹥”、“<”或“=”)。
②两溶液分别加入0.1 molNaOH固体,恢复到室温,Na2CO3溶液中的c(CO32-)____________(填“增大”、“减小”或“不变”);NaHCO3溶液中的c(HCO3-)_________(填“增大”、“减小”或“不变”)。
(3)常温下,甲为0.1 mol·L-1的HA溶液,pH﹥1;乙为0.1 mol·L-1的BOH溶液,且溶液中c(OH-):c(H+)=1012。请分别写出甲、乙两溶液中溶质的电离方程式:
甲__________________、乙_________________。
(4)相同条件下,对于浓度均为0.1 mol·L-1的NaCl溶液和CH3COONa溶液,溶液中的离子总数:NaCl溶液__________CH3COONa溶液(填“﹥”、“<”或“=”)。
(5)物质的量浓度相同的 ①氨水 ②氯化铵 ③碳酸氢铵 ④硫酸氢铵 ⑤硫酸铵五种溶液中c(NH4+)由大到小的顺序为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体内有20多种微量元素,它们的质量总和不到体重的千万分之一,但是对人的健康却起着重要的作用,下列各组元素全部是微量元素的是
A. Na、K、Cl、S、O
B. F、I、Fe、Zn、Cu
C. N、H、O、P、C
D. Ge、Ca、Cu、Mg、C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,反应后固体物质增重的是
A. 对氧化铁和碳的混合物高温加热
B. 石英、纯碱、石灰石的混合物高温制玻璃
C. 将铜丝烧红并迅速插入乙醇中充分反应
D. 将锌粒投入AgNO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物A2W和A2W2,E元素的周期序数与主族序数相等。
(1)E元素在周期表中的位置为________,W、D、E三种元素的简单离子的离子半径由大到小顺序为__________(用离子符号表示)。
(2)由A、B、W三种元素组成的18电子微粒的电子式为_______________。
(3)经测定A2W2为二元弱酸,其酸性比碳酸弱,写出其第一步电离的电离方程式_________________,实验室常用稀硫酸处理BaO2来制备A2W2,写出该反应的化学方程式_____________________________________。
(4)元素D的单质在一定条件下与元素A的单质化合生成一种化合物DA,熔点为800℃,DA能与水反应放氢气,该反应的化学方程式为____________。
(5)元素D的某化合物呈淡黄色,可与氯化亚铁溶液反应,生成红褐色沉淀,且无气体生成.则该反应的离子方程式为___________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com