
- 3 |
| A、21:5 | B、11:3 |
| C、3:1 | D、5:1 |
| 1 |
| 2 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、在常温下,Na2SiO3+H2O+CO2=Na2CO3+H2SiO3↓,说明H2CO3酸性强于H2SiO3;在高温下,Na2CO3+SiO2=Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3 |
| B、胶体区别于其他分散系的本质特点是能产生丁达尔现象 |
| C、KAl(SO4)2?12H2O是复盐;(NH4)2Fe(SO4)2也是复盐 |
| D、CaCl2、NaOH、HCl、HD四种物质都属于化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaO2的水解产物是Ca(OH)2和H2O2 |
| B、Mg3N2的水解产物是两种碱 |
| C、PCl3的水解产物是HClO和PH3 |
| D、CaC2的水解产物之一是C2H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、胆矾是电解质、液氨是非电解质 |
| B、淀粉溶液、硅酸、氯化铁溶液均为胶体 |
| C、淀粉、纤维素、油脂都属于天然高分子化合物 |
| D、SO3、SiO2、NO2均为酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下Na与足量的氧气反应生成Na2O,随温度升高生成Na2O的速率加快 |
| B、常温下pH=9的CH3COONa溶液和pH=9的NH3?H2O溶液,两溶液中水电离的c(H+)之比为104:1 |
| C、凡是放热反应都是自发进行的反应,而吸热反应都是非自发进行的反应 |
| D、pH=13的强碱溶液,加水稀释后,溶液中所有离子的浓度均变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、②③④ |
| C、③④⑤ | D、④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子式为C2H4Cl2的物质 |
| B、只含铁和氧两种元素且Fe的质量分数为72.41%的物质 |
| C、干冰 |
| D、按体积比为1:1混合NH3和HCl(同条件) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应属于氧化还原反应 |
| B、此反应中只有砷元素被氧化,只有氮元素被还原 |
| C、HNO3、H2O是反应物,H2SO4、NO、H3AsO4是生成物 |
| D、HNO3、H2SO4、H3AsO4都是最高价氧化物对应的水化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
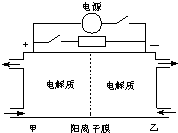 如图是一种蓄电池的示意图,被膜隔开的电解质分别为Na2S2和NaBr3.放电后变为Na2S4和NaBr下面对该装置工作过程中叙述正确的是( )
如图是一种蓄电池的示意图,被膜隔开的电解质分别为Na2S2和NaBr3.放电后变为Na2S4和NaBr下面对该装置工作过程中叙述正确的是( )| A、放电过程,甲电极电极反应:2S22--2e-=S42- |
| B、放电过程,电池反应:2S22-+Br3-=S42-+3Br- |
| C、充电过程,阳极室流出NaBr3溶液 |
| D、充电后向阳极室补充Na2S4溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com