
【题目】痛风病与关节滑液中形成的尿酸钠(NaUr)有关(NaUr增多,病情加重),其化学原理为:HUr(aq) + Na+ (aq)NaUr(s) + H+(aq)ΔH<0,下列说法不正确的是
A.炎热的夏季更易诱发关节疼痛
B.饮食中摄入过多食盐,会加重痛风病病情
C.患痛风病的人应少吃能代谢产生更多尿酸(HUr)的食物
D.大量饮水使 ![]() 增大,痛风病发作的可能性减小
增大,痛风病发作的可能性减小
【答案】A
【解析】
A.炎热的夏季温度较高,平衡逆向移动,使人体内尿酸钠(NaUr)含量减少,有利于缓解关节疼痛,故A错误;
B.饮食中摄入过多食盐,会增大Na+的浓度,使得平衡正向移动,人体中NaUr含量增多,会加重痛风病病情,故B正确;
C.若患痛风病的人应多吃能代谢产生更多尿酸的食物,会增大尿酸的浓度,使得平衡正向移动,人体中NaUr含量增多,病情加重,故患痛风病的人应少吃能代谢产生更多尿酸的食物,故C正确;
D.假设该反应中,c(H+)=c(NaUr)=c(Na+)=1mol/L,即K=![]() =1,饮水将各物质浓度稀释为0.01mol/L,则Qc=
=1,饮水将各物质浓度稀释为0.01mol/L,则Qc=![]() =100>K,
=100>K,![]() 增大,则平衡逆向移动,人体中NaUr含量会减少,降低痛风病发作的可能性,故D正确;
增大,则平衡逆向移动,人体中NaUr含量会减少,降低痛风病发作的可能性,故D正确;
答案选A。


科目:高中化学 来源: 题型:
【题目】Na2CO3与NaHCO3在生产、生活中用途非常广泛,同学们在实验室中探究Na2CO3和NaHCO3的性质。称取Na2CO3、NaHCO3固体各2g,分别加入两支大试管中,再各加10mL蒸馏水,充分溶解后,恢复至室温,各滴入2滴酚酞溶液,观察到如图所示现象。

(1)下列说法中,正确的是_____(填字母序号)。
a.两溶液中所含分子、离子种类完全相同
b.左侧试管中的现象解释了Na2CO3的俗名为什么叫做“纯碱”
c.向两支试管中加入过量硼酸饱和溶液,均有无色气体生成
(2)两溶液中的离子浓度都存在下式的数量关系,请你补充完整:c(Na+)+c(H+)=_____。
(3)NaHCO3溶液中存在下列两种变化趋势:
变化i.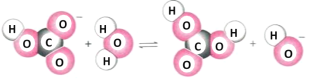
变化ii.(用离子方程式表示)_____。
溶液中滴加酚酞变为粉色,是因为以_____为主(填“变化i”或“变化ii”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是()
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是()
A | B | C | D |
|
|
|
|
升高温度,正反应方向平衡常数减小 | 0~3s内,反应速率为:v(NO2)=0.2 mol·L-1·s-1 | t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜板上铁铆钉处的吸氧腐蚀原理如图所示,下列有关说法中,不正确的是

A. 正极电极反应式为:2H++2e—→H2↑
B. 此过程中还涉及到反应:4Fe(OH)2+2H2O+O2=4Fe(OH)3
C. 此过程中铜并不被腐蚀
D. 此过程中电子从Fe移向Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示。下列说法正确的是( )

A.化合物RX中含共价键
B.化合物X2M是非电解质
C.M的单质在常温常压下为气体
D.Y形成的化合物种类最多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图完成一氧化氮与过氧化钠反应制备亚硝酸钠(2NO+Na2O2=2NaNO2,2NO2+Na2O2=2NaNO3,NO能被酸性KMnO4溶液氧化为NO3-),下列说法错误的是

A.检查装置气密性后,应先打开止水夹,从导管中通入N2
B.装置C是用来吸收CO2的
C.D管中可能含有的杂质为NaNO3、NaOH
D.装置E用于处理尾气,反应中氧化剂与还原剂的物质的量之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色溶液中可能含有Na+、K+、NH4+、Ca2+、Cu2+、SO42—、SO32—、Cl-、Br-、CO32—中的若干种,离子浓度都为0.1 mol·L-1。往该溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成。某同学另取少量原溶液,设计并完成如图所示实验。则下列关于原溶液的判断正确的是( )
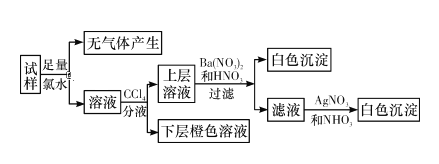
A.若实验中Ba(NO3)2和HNO3的混合溶液改用BaCl2和盐酸的混合溶液,对溶液中离子的判断无影响
B.无法确定原溶液中是否存在Cl-
C.原溶液中肯定存在的上述离子是SO32—、Br-,是否存在Na+、K+需要通过焰色反应来确定
D.原溶液中肯定不存在的上述离子是Ca2+、Cu2+、SO42—、CO32—,是否存在NH4+另需实验验证
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车剧烈碰撞时,安全气囊中发生反应![]() 。若有2 mol N2生成,则下列判断正确的是( )
。若有2 mol N2生成,则下列判断正确的是( )
A.N2的体积为44. 8 L
B.有 0. 125 mol KNO3被氧化
C.N2既是氧化产物又是还原产物
D.转移电子的物质的量为10 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a~n10中元素在周期表中的位置如图所示,请回答下列问题:
a | ||||||||
b | c | d | e | |||||
f | g | h | m | n | ||||
…… |
(1)m的阴离子的结构示意图为___。
(2)b的最高价氧化物的化学式为___;用化学方程式表示f、d的单质形成f2d2的过程___。
(3)d、g、n形成的简单离子的半径由大到小的顺序为___(用离子符号表示)。
(4)以上元素组成的物质有下列框图中的转化关系,其中甲为10电子微粒。
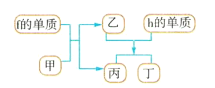
请写出h的单质与乙反应的化学方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com