
��12�֣���һ�ݻ�Ϊ2 L���ܱ������У�����0.2 mol��N2��0.6 mol��H2����һ�������·�����Ӧ��N2(g)��3H2(g) 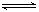 2NH3(g)����H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺
2NH3(g)����H��0 ����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺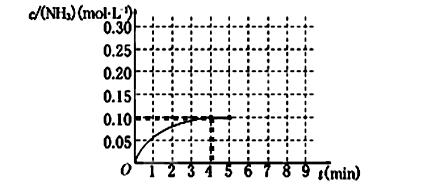
��1��������ͼ������ӷ�Ӧ��ʼ��ƽ��ʱ��������ƽ����Ӧ����v(H2)Ϊ______________��
��2���÷�Ӧ�ﵽƽ��ʱN2��ת����_________________��
��3����Ӧ�ﵽƽ���5����ĩ�����������������䣬���ı䷴Ӧ�¶ȣ���NH3�����ʵ���Ũ�Ȳ�����Ϊ____________��(�����)
a��0.20 mol��L��1 b��0.12 mol��L��1 c��0.10 mol��L��1 d��0.08 mol��L��1
��4����д���÷�Ӧ��ƽ�ⳣ������ʽ_________�����÷�Ӧ��298K��398Kʱ�Ļ�ѧƽ�ⳣ���ֱ�ΪK1��K2����K1 K2�����������="��" �� ������ ����
��5���ڵ�5����ĩ�������������Сһ������ڵ�8����ĩ�ﵽ�µ�ƽ��(��ʱNH3��Ũ��ԼΪ0.25 mol��L��1)��������ͼ�л�����5����ĩ����ƽ��ʱNH3Ũ�ȵı仯���ߡ�
��1��0.0375 mol��L��1��min��1
��2��50%
��3��a��c
��4��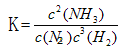 >
>
��5��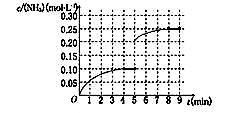
���������������1������v��H2��= 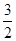 c��NH3�����м��㣬v��H2��=
c��NH3�����м��㣬v��H2��= 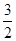 c��NH3��=
c��NH3��=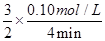 =0.0375 mol��L��1��min��1
=0.0375 mol��L��1��min��1
��2�����ݰ�����Ũ��������ɰ��������ʵ���Ϊ0.2mol����Ӧ�ĵ���Ϊ0.1mol��ת����Ϊ50%��
��3���÷�ӦΪ���淴Ӧ����Ӧ�ﲻ������ȫת������NH3�����ʵ���Ũ�Ȳ�����Ϊ0.2mol/L���¶ȸı�ƽ��һ�������ƶ�����NH3�����ʵ���Ũ�Ȳ�����Ϊ0.1mol/L���ʴ�Ϊ��a��c��
��4��ƽ�ⳣ�������������Ũ����֮�����Է�Ӧ���Ũ����֮����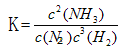 ����Ϊ�÷�Ӧ�Ƿ��ȷ�Ӧ���¶�Խ�ߣ�KֵԽС��K1>K2��
����Ϊ�÷�Ӧ�Ƿ��ȷ�Ӧ���¶�Խ�ߣ�KֵԽС��K1>K2��
��5����5����ĩ�������������Сһ�������Ũ��Ϊԭ����һ����ѹǿ����ƽ�����������ƶ���������Ũ��������8minʱ�ﵽƽ�⣬Ũ��ԼΪ0.25mol/L����ͼ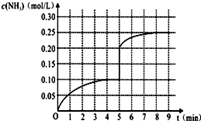
���㣺��ѧƽ�ⳣ���ĺ��壻��Ӧ���ʵĶ�����ʾ��������ѧƽ���Ӱ�����أ���ѧƽ��״̬���жϡ�
���������⿼�黯ѧƽ���ƶ����⣬�漰ƽ�ⳣ������Ӧ���ʡ�ƽ���־�Լ�ƽ��ͼ������⣬��Ŀ�Ѷ��еȣ�ע�ⷽ��������Ļ��ۡ�


 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��9�֣���һ�ݻ�Ϊ2 L���ܱ������ڼ���0.2 mol��N2��0.6 mol��H2����һ�������·������·�Ӧ��N2(g)��3H2(g)![]() 2NH3(g) ��H<0����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��
2NH3(g) ��H<0����Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��
��ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ��K����ʽΪ______________________��
�����¶�Kֵ ����������С�����䡱��
��2��������ͼ������ӷ�Ӧ��ʼ��ƽ��ʱ��ƽ����Ӧ����v(H2)Ϊ____________��
��3���жϸ÷�Ӧ�ﵽƽ��״̬�ı�־�� ������ĸ����
a��N2��NH3Ũ����� b��NH3�ٷֺ������ֲ���
c�������������ѹǿ���� d��NH3������������H2�������������
e�������л��������ܶȱ��ֲ���
��4����Ӧ�ﵽƽ���5����ĩ�����������������䣬���ı䷴Ӧ�¶ȣ���NH3�����ʵ���Ũ�Ȳ�����Ϊ_______________��
a. 0.20 mol/L b. 0.12 mol/L c.0.10 mol/L d.0.08 mol/L
��5���ڵ�5����ĩ�������������Сһ������ڵ�8����ĩ�ﵽ�µ�ƽ�⣨��ʱNH3��Ũ��ԼΪ0.25mol/L����������ͼ�л�����5����ĩ�ﵽ��ƽ��ʱNH3Ũ�ȵı仯���ߡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�긣��ʡ������������ѧ�߶���ѧ�ڵ�һ���¿���ѧ�Ծ����������� ���ͣ������
(16��)���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã��ϳɰ���ҵ�ڹ�������������Ҫ���塣�����ǹ��ںϳɰ����й����⣬��ش�
��1������һ�ݻ�Ϊ2 L���ܱ������м���0.2 mol��N2��0.6 mol��H2��һ�������·�����Ӧ: N2(g) +3H2(g) 2NH3(g) ��H<0������5����ʱ��Ӧ�ﵽƽ�⣬��ʱ���NH3�����ʵ���Ϊ0.2 mol����ǰ5���ӵ�ƽ����Ӧ����v(N2)= ��ƽ��ʱH2��ת����Ϊ ��?
2NH3(g) ��H<0������5����ʱ��Ӧ�ﵽƽ�⣬��ʱ���NH3�����ʵ���Ϊ0.2 mol����ǰ5���ӵ�ƽ����Ӧ����v(N2)= ��ƽ��ʱH2��ת����Ϊ ��?
��2��ƽ�����Ҫ���H2��ת���ʣ����Բ�ȡ�Ĵ�ʩ�� ��?
A.���˴��� B.�����������?C.���ͷ�Ӧ��ϵ���¶� D.����һ����N2?
��3������0.5 L���ܱ������У�һ�����ĵ����������������·�Ӧ��?
N2(g)+3H2(g) 2NH3(g) ��H<0���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ�����ʾ��?
2NH3(g) ��H<0���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ�����ʾ��?
| T/�� | 200 | 300 | 400 |
| K | K1 | K3 | 0.5 |
 N2(g)+3H2(g)�Ļ�ѧƽ�ⳣ��Ϊ �������NH3��N2��H2���ʵ����ֱ�Ϊ3 mol��2 mol�� 1 molʱ����÷�Ӧ��v(N2)�� v(N2)�����<����>����������?
N2(g)+3H2(g)�Ļ�ѧƽ�ⳣ��Ϊ �������NH3��N2��H2���ʵ����ֱ�Ϊ3 mol��2 mol�� 1 molʱ����÷�Ӧ��v(N2)�� v(N2)�����<����>����������?�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�꽭��ʡ�������������߶���ѧ�����п��Ի�ѧ�Ծ����������� ���ͣ������
��10�֣���һ�ݻ�Ϊ2 L���ܱ������м���2 molA��3 molB�������¶�Ϊ30�棬�ڴ������ڵ������½������з�Ӧ��A(g)+2B(g) 3C(g)���ﵽƽ�������1.5 mol C����ʱ��ƽ��������C���������Ϊ�أ������¶����ߵ�70����������������䣬����Ӧ���´ﵽƽ��ʱ��C�����ʵ���Ϊ1.2 mol��
3C(g)���ﵽƽ�������1.5 mol C����ʱ��ƽ��������C���������Ϊ�أ������¶����ߵ�70����������������䣬����Ӧ���´ﵽƽ��ʱ��C�����ʵ���Ϊ1.2 mol��
��ش��������⣬
��1���÷�Ӧ���ʱ��H 0(�>������<����=��)��
��2��30��ʱ��ƽ��������C�����������= ��A���ʵ�ת������B���ʵ�ת����֮��Ϊ ��
��3��30��ʱ������ͬһ�����м���1.5 mol A�� mol B��1.5 mol C����ƽ��������C�����������Ϊ�أ���ʱƽ����ϵ��A�����ʵ���Ũ��Ϊ mol��L��1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���Ĵ�ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
(10��)��һ�ݻ�Ϊ2 L���ܱ������У�����0.2 mol��N2��0.6 mol��H2����һ�������·�����Ӧ��N2(g)��3H2(g)  2NH3(g)����H��0
2NH3(g)����H��0
��Ӧ��NH3�����ʵ���Ũ�ȵı仯�������ͼ��ʾ����ش��������⣺

(1)������ͼ������ӷ�Ӧ��ʼ��ƽ��ʱ��ƽ����Ӧ����v(NH3)Ϊ______________��
(2)�÷�Ӧ�ﵽƽ��ʱH2��ת����________��
(3)��Ӧ�ﵽƽ���5����ĩ�����������������䣬���ı䷴Ӧ�¶ȣ��ﵽ��ƽ��ʱNH3�����ʵ���Ũ�Ȳ�����Ϊ____________��(�����)
A��0.20 mol��L��1 b��0.12 mol��L��1 c��0.10 mol��L��1 d��0.08 mol��L��1
(4)�ڵ�5����ĩ�������������Сһ������ڵ�8����ĩ�ﵽ�µ�ƽ��(��ʱNH3��Ũ��ԼΪ0.25 mol��L��1)��������ͼ�л�����5����ĩ����ƽ��ʱNH3Ũ�ȵı仯���ߣ�
��5�����������Ӧ����ͬ�¶Ⱥ������н��У���ʹ��Ӧ�ﵽƽ��ʱNH3�����ʵ���������ԭƽ����ȣ���ʼ������������ʵ����ʵ���n��N2����n��H2����n��NH3���ֱ�Ϊa��b��c����a��b��c֮��Ӧ������Ĺ�ϵʽΪ��
(6)���÷�Ӧ��298K��398Kʱ�Ļ�ѧƽ�ⳣ���ֱ�ΪK1��K2����K1 K2������� ��=�� �� ������ ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013��㶫ʡ�߶���ѧ�����п��Ի�ѧ�Ծ� ���ͣ������
��20�֣���һ�ݻ�Ϊ2 L���ܱ������ڼ���0.2 mol ��N2��0.6 mol ��H2����һ�������·������·�Ӧ��N2(g)��3H2(g) 2NH3(g) ��H��0,��Ӧ��NH3�����ʵ���Ũ�ȵı仯���������ͼ��
2NH3(g) ��H��0,��Ӧ��NH3�����ʵ���Ũ�ȵı仯���������ͼ��

��1��������ͼ������ӷ�Ӧ��ʼ��ƽ��ʱ��ƽ����Ӧ����v(NH3)Ϊ____ _��
��2���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽK = ____ _ ��
��3����Ӧ�ﵽƽ���5����ĩ�����������������䣬���ı䷴Ӧ�¶ȣ���NH3�����ʵ���Ũ�Ȳ�����Ϊ________��
a. 0.20 mol/L b. 0.12 mol/L c. 0.10 mol/L d. 0.08 mol/L
��4����Ӧ�ﵽƽ���5����ĩ�����������������䣬��ֻ�������������Сһ�룬ƽ��_________________________�ƶ�������淴Ӧ������������Ӧ������������ѧƽ�ⳣ��________________�����������С�����䡱����
��5���ڵ�5����ĩ�������������Сһ������ڵ�8����ĩ�ﵽ�µ�ƽ�⣨��ʱNH3��Ũ��ԼΪ0.25 mol/L����������ͼ�л�����5����ĩ����ƽ��ʱNH3Ũ�ȵı仯���ߡ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com