
【题目】下列实验现象预测正确的是( )
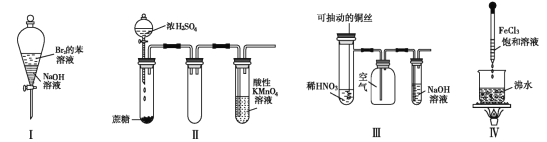
A. 实验Ⅰ:振荡后静置,上层溶液颜色保持不变
B. 实验Ⅱ :酸性 KMnO4 溶液中出现气泡,且颜色逐渐褪去
C. 实验Ⅲ:微热稀 HNO3 片刻,溶液中有气泡产生,广口瓶内始终保持无色
D. 实验Ⅳ:滴入 FeCl3 后,可形成带电的胶体,该分散系导电能力增强
【答案】B
【解析】A.根据单质溴能与NaOH溶液发生反应,苯与水互不相溶;B.根据浓硫酸具有脱水性和氧化性的性质分析;C.根据在加热时稀硝酸与铜发生反应,硝酸被还原成NO,广口瓶内有空气,可与NO反应;D.胶体粒子带电荷,胶体本身不带电。
A项,苯的密度比水小,位于上层,苯中的Br2与NaOH溶液发生反应,因此振荡后静置,上层溶液褪色,故A项错误;
B项,浓H2SO4与蔗糖发生氧化还原反应生成SO2和CO2,CO2不与酸性KMnO4溶液反应,有气泡产生,SO2与酸性KMnO4溶液发生氧化还原反应使溶液褪色,故B项正确;
C项,微热稀HNO3片刻,铜与稀HNO3发生反应生成NO,NO与广口瓶内的O2反应生成红棕色的NO2,故C项错误。
D项,FeCl3饱和溶液滴入沸水中继续煮沸至红褐色,生成氢氧化铁胶体,胶体电中性,不带电,故D项错误;
综上所述,本题正确答案为B。


 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法错误的是
A.SO2可用作食品漂白剂B.乙烯可以用作生产食品包装材料的原料
C.酒越陈越香与酯化反应有关D.75%的酒精为消毒酒精
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物a的分子式和己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是( )
A.a分子中可能有三个甲基
B.a的分子式为C6H10
C.a的一氯代物可能有三种
D.a能与溴的四氯化碳溶液发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏伽德罗常数.已知C2H4和C3H6的混合物的质量为ag,则该混合物( )
A.所含共用电子对数目为( ![]() +1)NA
+1)NA
B.所含碳氢键数目为 ![]()
C.燃烧时消耗的O2一定是33.6a/14L
D.所含原子总数为 ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】活性氧化锌(ZnO)粒径介于1-100 nm之间,是一种面向21世纪的新型高功能精细无机产品,表现出许多特殊的性质。某研究所以粗氧化锌(含少量CuO、FeO、MnO、Fe2O3等)为原料,采用湿化学法(NPP-法)制备纳米级活性氧化锌,生产工艺流程如图:
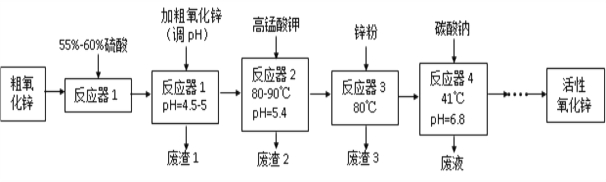
已知:
①pH=5.4时,KMnO4的还原产物为MnO2。
②以上实验条件下各种氢氧化物沉淀的pH情况如下表所示。
Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Mn(OH)2 | |
开始沉淀的pH | 7.5 | 2.2 | 5.2 | 6.4 | 8.6 |
沉淀完全的pH | 9.0 | 3.2 | 6.7 | 8.0 | 10.1 |
根据以上信息,回答下列问题:
(1)工艺过程中各步骤均用到的分离方法是_______________________________。
(2)“废渣1”的主要成分是______________________________________________。
(3)“反应器2”中两个氧化还原反应的离子方程式为_______________________________________________________________
(4) “反应器3”中加入锌粉的作用是________________________________。
(5)“反应器4”得到的废液中,含有的主要离子除了Na+外,还有______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】变量控制是科学研究的重要方法。相同质量的碳酸钙与足量1 mol·L-1盐酸分别在下列条件下发生反应,化学反应速率最大的是
选项 | 碳酸钙的状态 | 实验温度/℃ |
A | 粉末 | 10 |
B | 粉末 | 30 |
C | 块状 | 10 |
D | 块状 | 30 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在2L恒容密闭容器中,发生反应2NO(g)+O2(g)2NO2(g).
①某温度时,按物质的量比2:1充入NO和O2开始反应,n(NO)随时间变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.007 | 0.006 | 0.006 | 0.006 |
0~4s内以O2浓度变化表示的反应速率为________.
②能说明该反应已达到平衡状态的是________.
A.气体颜色保持不变 B.气体平均相对分子质量保持不变
C.υ正(NO)=2υ正(O2) D.气体压强保持不变
③已知:K300℃>K400℃.下列措施能使该反应的反应速率增大且平衡向正反应方向移动的是_______.
A、升高温度 B、充入Ar使压强增大
C、选择高效催化剂 D、充入NO使压强增大
(2)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解100ml 1mol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24L(设电解后溶液体积不变).

①甲烷燃料电池的负极反应式:____________________________________________.
②电解后溶液的pH=________(忽略氯气与氢氧化钠溶液反应).
(3)在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题:

①下列3个反应中符合示意图描述的反应的是 ___________(填代号).
A、铝粉与Fe2O3反应 B、用水稀释浓硫酸溶液 C、灼热的碳与CO2反应
②以甲烷为原料制取氢气是工业上常用的制氢方法.已知:
CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+306kJ/mol
CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=+240kJ/mol
CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为_______________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把等量金属钠进行下列实验,其中生成氢气最多的是
A.把钠放入足量稀盐酸中B.把钠放入足量水中
C.把钠放入硫酸铜溶液中D.将钠用铝箔包好并刺些小孔,再放入水中
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com