
����Ŀ����������п(ZnO)��������1-100 nm֮�䣬��һ������21���͵����߹��ܾ�ϸ����Ʒ�����ֳ�������������ʡ�ij�о����Դ�����п��������CuO��FeO��MnO��Fe2O3�ȣ�Ϊԭ�ϣ�����ʪ��ѧ��(NPP-��)�Ʊ�������������п����������������ͼ��
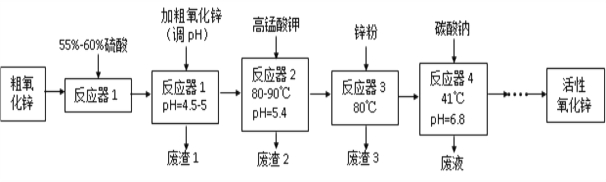
��֪��
��pH=5.4ʱ��KMnO4�Ļ�ԭ����ΪMnO2��
������ʵ�������¸����������������pH������±���ʾ��
Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Zn(OH)2 | Mn(OH)2 | |
��ʼ������pH | 7.5 | 2.2 | 5.2 | 6.4 | 8.6 |
������ȫ��pH | 9.0 | 3.2 | 6.7 | 8.0 | 10.1 |
����������Ϣ���ش��������⣺
��1�����չ����и�������õ��ķ��뷽����_______________________________��
��2��������1������Ҫ�ɷ���______________________________________________��
��3������Ӧ��2��������������ԭ��Ӧ�����ӷ���ʽΪ_______________________________________________________________
��4�� ����Ӧ��3���м���п�۵�������________________________________��
��5������Ӧ��4���õ��ķ�Һ�У����е���Ҫ���ӳ���Na+�⣬����______________��
���𰸡� ���� Fe(OH)3 MnO4�� + 3Fe2+ + 4H+ = 3Fe3+ + MnO2��+ 2H2O��2MnO4�� +3Mn2++2H2O = 5MnO2��+ 4H+ ��ȥ��Һ��Cu2+ K+��SO42��
����������1�����⿼�����ʵij��Ӻͷ��룬�������̣�������õ�������Һ����������˷��뷽���ǹ��ˣ���2�����⿼�����ܵ�����ܽ�ƽ���Ӧ�ã���Ӧ��1���Ӵ�����п��Ŀ���ǵ���pH������4.5��5�����ݱ������ݣ�Fe3����������������ʽ����������������1ΪFe(OH)3����3�����⿼��������ԭ��Ӧ����ʽ����д�����ݴ�����п�ijɷ֣���Ӧ��1�к���Fe2������˼�����������Һ��Ŀ��֮һ�ǰ�Fe2��������Fe3����Ȼ�����pH����ȥ��������ӷ�Ӧ����ʽΪMnO4�� + 3Fe2�� + 4H�� = 3Fe3�� + MnO2��+ 2H2O�����ݴ�����п�ijɷ֣���Ӧ��1�еõ������ӻ�����Mn2������������ͼ���������Ը��������Һ��Ŀ��֮���dz�ȥMn2�������ӷ�Ӧ����ʽΪ2MnO4�� +3Mn2��+2H2O = 5MnO2��+ 4H�� ����4���������ʵij��ӣ������̵�Ŀ���ǵõ���������п�����ݷ�Ӧ��1��2����Ӧ��3��Ŀ���dz�ȥCu2����������ý�����ԣ�����Zn��Cu2��=Zn2��Cu������п��Ŀ���dz�ȥ��Һ��Cu2������5���������ӵĴ��ڣ���������ͼ����Ӧ��4�еķ�Һ�к���Na����K����SO42���ȡ�


 ���ĺ����Ͼ�������ϵ�д�
���ĺ����Ͼ�������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������л���ѧ����ʶ�У��������
A. ��Ӧ ![]() ����ȡ����Ӧ
����ȡ����Ӧ
B. ���ۺ���ά�����ڶ��ǣ���������ˮ��ת��Ϊ�����ǣ�Ϊ�����ṩ����
C. ��֦��ṹ��ʽ��ͼ �������Ҵ������ᷴӦ��Ҳ��ʹ������Ȼ�̼��Һ�����Ը��������Һ��ɫ
�������Ҵ������ᷴӦ��Ҳ��ʹ������Ȼ�̼��Һ�����Ը��������Һ��ɫ
D. ȡ����ˮ��Һ�������ȵμӹ�����NaOH��Һ���ٵ������Ƶ�������ͭ����Һ�����ȣ��к�ɫ�������ɣ�֤����ˮ�������л�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���3 mol A��1 mol B�����������ڹ̶��ݻ�Ϊ2 L���ܱ������У��������·�Ӧ��3A��g����B��g��![]() xC��g����2D��g����2 minĩ�÷�Ӧ�ﵽƽ�⣬�������0.8 mol D�� 0.4 mol C�������ж�����ȷ����
xC��g����2D��g����2 minĩ�÷�Ӧ�ﵽƽ�⣬�������0.8 mol D�� 0.4 mol C�������ж�����ȷ����
A. x ��1
B. 2 minʱ��A��Ũ��Ϊ0.9mol��L-1
C. 2 min��A�ķ�Ӧ����Ϊ0.3 mol��L-1��min-1
D. B��ת����Ϊ60%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���0.100 mol��L��1 NaOH��Һ�ֱ�ζ�20.00 mL 0.100 mol��L��1������ʹ��ᣬ�ζ�������ͼ��ʾ������˵����ȷ����(����)

A. ����ʾ���ǵζ����������
B. pH��7ʱ���ζ��������ĵ�V(NaOH)С��20 mL
C. V(NaOH)��20.00 mLʱ��������Һ��c(Cl��)��c(CH3COO��)
D. V(NaOH)��10.00 mLʱ��������Һ��c(Na��)>c(CH3COO��)>c(H��)>c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016��9���ҹ��ɹ����ô������ػ�����䡰�칬���š��ռ�ʵ���ҡ�����ƽ�����װ�л�ԭ���£�N2H4����Һ̬����ǿ�������������⣨H2O2������ͼ��һ��������ȫ��Ӧ���ɵ�����ˮ�����е������仯ͼ����ش��������⣺
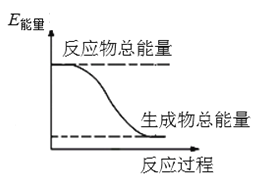
��1�����������������Ʋ����Ľṹʽ��__________________________��
��2��Һ̬�����������ķ�Ӧ����________������ȡ����ȡ�����Ӧ��
��3��д���û���ƽ�������ط�Ӧ�Ļ�ѧ����ʽ��_____________________��
��4����֪�º������ɷ������·�Ӧ��N2H4��g��+O2��g��N2��g��+2H2O��g��
��ij�¶��£��ݻ��̶����ܱ������У�����������˵��������Ӧ�ﵽƽ�����______��
A. �ԣ�N2�� = �ԣ�N2H4��
B. c��N2H4�� : c��O2�� : c��N2�� = 1:1:1
C. ���������ܶȲ��ٷ����仯
D. ��ϵ��ѹǿ���ٷ����仯
E. ��������ƽ����Է����������ٷ����仯
F. ÿ�Ͽ�1 mol O=O����ͬʱ�Ͽ�4 mol H-O��
������Ҫ���Ӹ÷�Ӧ������Ӧ���ʣ�����Ϊһ�����еķ����У�____________��
A. ���߷�Ӧ�¶� B. �����ʵ��Ĵ���
C. ������������� D. �������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������Ԥ����ȷ����( )
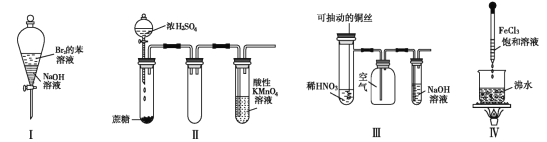
A. ʵ������ã��ϲ���Һ��ɫ���ֲ���
B. ʵ��� ������ KMnO4 ��Һ�г������ݣ�����ɫ����ȥ
C. ʵ�����ϡ HNO3 Ƭ�̣���Һ�������ݲ��������ƿ��ʼ�ձ�����ɫ
D. ʵ��������� FeCl3 ���γɴ���Ľ��壬�÷�ɢϵ����������ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������������ռ����Ҫ�ĵ�λ���������е���һЩ��Ȼ�Ļ�ϳɵĴ������ϣ�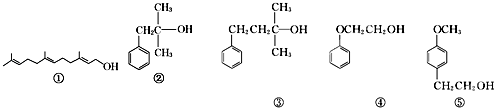
����˵������ȷ���ǣ�������
A.��������KMnO4��Һ��������Ƿ���̼̼˫��
B.�ں͢ۻ�Ϊͬϵ����ܴ���������ȩ
C.�ܺ͢ݻ�Ϊͬϵ����ú˴Ź���������
D.�����ʵ���������5���л����������Ľ����Ʒ�Ӧ�������Ƶ�����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʯ�ǹ�ҵ��������Ҫԭ��֮һ������Ҫ�ɷ�Ϊ����������(�������в�����Ԫ�غ���Ԫ�أ������ʲ���H2SO4��Ӧ)��ij�о���ѧϰС���ij����ʯ������������Ļ�ѧʽ����̽����
I������ʯ�к������IJⶨ
�ٰ���ͼ��װ���������װ�õ������ԣ�
�ڽ� 10.0g ����ʯ����Ӳ�ʲ������У�װ��B��C�е�ҩƷ��ͼ��ʾ���г�������ʡ�ԣ���
�۴���˵����ܿڴ����ϵ�ͨ�� H2��______����ȼ A ���ƾ��ƣ�
�ܡ���
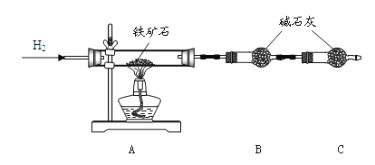
(1)װ�� C ������Ϊ_______________________________________ ��
(2)������۵IJ�������������_________��
(3)ʵ�������IJ��������� a.��ȴ������ b.Ϩ�� A ���ľƾ��� c.ֹͣͨ H2����ȷ��˳��Ϊ��_________������ţ���
(4)ʵ���÷�Ӧ��װ�� B���� 2.7g���ݴ˿��Բ������ʯ�����ĺ�������ͬѧ��Ϊ�����ⶨ B װ�õľ���������ͨ���ⶨ_________��Ҳ�ܴﵽʵ��Ŀ�ġ�
II������ʯ�к������IJⶨ
������ʵ�������Ӳ�ʲ������еĹ���ȫ��ȡ����������ϡ�����ȡ����ˡ�����Һ��ͨ������Cl2 ��������е���Һ M����ȴ����Һ M ϡ���� 250mL��ȡ 20.00mL M ��ϡ��Һ���� 0.5000mol��L-1�ı� KI ��Һ���䷴Ӧ������ KI ��Һ 20.00 mL��
(5)����Һ��ͨ������ Cl2 ��Ŀ���ǽ����е� Fe2+������ Fe3+����ͨ�� Cl2 �����Һ������е�Ŀ������_________�� ��ʡȥ�ò��������������İٷֺ�����_________�����ƫ�� ��ƫС������Ӱ�족����
(6)�� KI ��Һ�� M ϡ��Һ������Ӧ�����ӷ���ʽΪ��_________��
III����ѧʽ��ȷ��
(7)��� I�� II ��ʵ�����ݼ��������ʯ������������Ļ�ѧʽΪ_________�� (�뻯�����������)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��̬��A���ܶ�����ͬ״���������ܶȵ�14�����л���A~E�ܷ�����ͼ��ʾһϵ�б仯��������˵���������
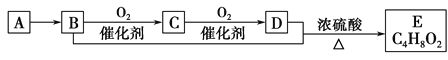
A. A����������ԭ�Ӿ���ͬһƽ����
B. C4H8O2��������ͬ���칹����4��
C. C��ˮ��Һ�ֳƸ������֣�����ɱ������������
D. �����ʵ�����B��D�������Ʒ�Ӧ��������������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com